|
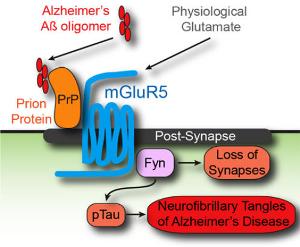
Растворимые олигомеры бета-амилоида (Aβ) являются триггером патофизиологии болезни Альцгеймера и связываются с высокой аффинностью с клеточным прионным белком (PrP). Связанный с PrP внеклеточной Aβ активирует внутриклеточную киназу Fyn, разрушая синапсы. Активация киназы Fyn связанным с PrP Aβ происходит только при ко-экспрессии метаботропных рецепторов глутамата, mGluR5. PrP и mGluR5 взаимодействуют физически, и цитоплазматическая Fyn образует комплекс с mGluR5. Взаимодействие Aβ-PrP приводит к mGluR5-опосредованному повышению уровня внутриклеточного кальция в ооцитах и нейронах Xenopus. Кроме того, сигналинг комплексов Aβ-PrP-mGluR5 опосредует фосфорилирование eEF2 и потерю дендритных шипиков. Таким образом, Aβ-PrP-комплексы на поверхности нейронов активируют mGluR5, нарушая функцию нейронов. У мышей, экспрессирующих трансгены семейной болезни Альцгеймера, антагонисты mGluR5 обращают вспять нарушение памяти, способности к обучению и снижение плотности синапсов. (Рис. Yale University)
Ученые Школы медицины Йельского университета (Yale University School of Medicine) установили белок, являющийся недостающим звеном в сложной цепи молекулярных событий, ведущих к развитию болезни Альцгеймера. Блокирование этого белка одним из существующих препаратов восстанавливает память у мышей с повреждением головного мозга, имитирующим это заболевание.
«Очень интересно то, что из всех звеньев этой молекулярной цепи именно этот белок может быть наиболее легко достижимой мишенью препаратов», - говорит руководитель исследования профессор неврологии Стивен Стриттмэттер (Stephen Strittmatter). «Это дает нам твердую надежду, что мы сможем найти препарат, который облегчит бремя болезни Альцгеймера».
Ученые уже составили частичную молекулярную карту того, как болезнь Альцгеймера разрушает клетки головного мозга. В своей более ранней работе лаборатория профессора Стриттмэттера показала, что бета-амилоидные пептиды, являющиеся характерным признаком болезни Альцгеймера, взаимодействуют с прионными белками на поверхности нейронов. Это взаимодействие активирует внутриклеточный молекулярный мессенджер, киназу Fyn, хотя точный механизм этой активации оставался неизвестным.
В своем последнем исследовании профессор Стриттмэттер и его коллеги определили недостающее звено этой цепи – мембранный белок, называемый метаботропным рецептором глутамата 5 (metabotropic glutamate receptor 5, mGluR5.) Блокирование этого белка препаратом, близким к разработанному для лечения синдрома фрагильной Х-хромосомы, восстанавливает память, способность к обучению и плотность синапсов в мышиной модели болезни Альцгеймера.
Как подчеркивает Стриттмэттер, новые препараты можно разработать таким образом, что их мишенью будут именно рецепторы mGluR5. Сейчас его лаборатория ищет пути к достижению этой цели.
По материалам
Alzheimer’s missing link found: Is a promising target for new drugs
Оригинальная статья:
Ji Won Um, Adam C. Kaufman, Mikhail Kostylev, Jacqueline K. Heiss, Massimiliano Stagi, Hideyuki Takahashi, Meghan E. Kerrisk, Alexander Vortmeyer, Thomas Wisniewski, Anthony J. Koleske, Erik C. Gunther, Haakon B. Nygaard, Stephen M. Strittmatter. Metabotropic Glutamate Receptor 5 Is a Coreceptor for Alzheimer Aβ Oligomer Bound to Cellular Prion Protein
© «Найденное недостающее звено в развитии болезни Альцгеймера – перспективная мишень будущих препаратов». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Болезнь Альцгеймера.
Related Articles: |













