|
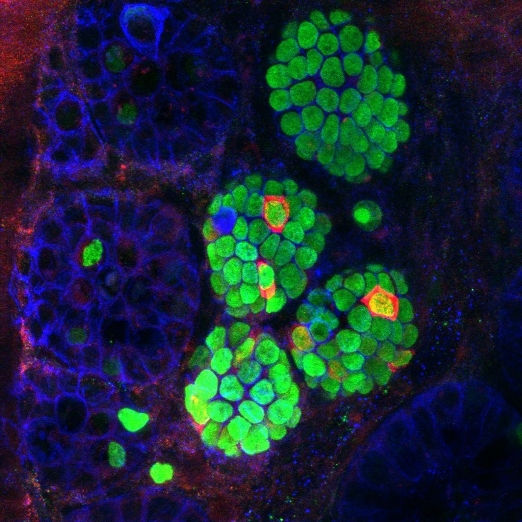
Инсулин-экспрессирующие клетки (красные), появляющиеся среди клеток кишечных крипт мыши (зеленые), получившей три фактора перепрограммирования в бета-клетки. (Фото: Ben Stanger, MD, PhD, Perelman School of Medicine)
Гибель производящих инсулин бета-клеток поджелудочной железы лежит в основе диабета 1-го и 2 типов. «Мы ищем пути получения новых бета-клеток для этих пациентов, чтобы в один прекрасный день заменить ими ежедневные инъекции инсулина», - говорит руководитель исследования Бен Стэнджер (Ben Stanger), MD, PhD, доцент кафедры медицины отделения гастроэнтерологии Школы медицины Перельмана (Perelman School of Medicine) Пенсильванского университета (University of Pennsylvania).
Одним из подходов к лечению этой болезни является пересадка островковых клеток больным с тяжелым диабетом 1 типа для восстановления нормального уровня сахара в крови. Еще одной областью исследования является использование стволовых клеток для получения из них бета-клеток. Однако обе эти стратегии имеют ограничения: островковые клетки в дефиците, а основанным на стволовых клетках подходам еще предстоит пройти долгий путь, прежде чем их можно будет использовать в клинике.
«Использовать правильное сочетание транскрипционных факторов для трансформации любой клетки в клетку любого другого типа – мощная идея. Это клеточная алхимия», - комментирует доктор Стэнджер.
Новое исследование доктора Стэнджера и постдокторанта И-Цзюй Чен (Yi-Ju Chen), PhD, опубликованное в журнале Cell Reports, доказывает, что введение трех белков, управляющих регуляцией ДНК в ядре, – так называемых транскрипционных факторов – иммуннодефицитным мышам трансформирует специфическую группу клеток слизистой оболочки кишечника в клетки, близкие к инсулин-продуцирующим бета-клеткам. Эта работа открывает перспективы использования дифференцированных клеток поджелудочной железы в качестве источника новых бета-клеток.
В 2008 году лаборатория научного руководителя доктора Стэнджера ввела три фактора, ответственных за перепрограммирование в бета-клетки – Pdx1 (P), MafA (М), и Ngn3 (N) – вместе называемых PMN, – в ацинарные клетки поджелудочной железы. Эта манипуляция привела к появлению у ацинарных клеток некоторых структурных и физиологических особенностей бета-клеток.
Основываясь на результатах этого исследования, группа Стэнджера поставила своей целью определить, какие другие типы клеток, если таковые существуют, могут быть перепрограммированы в бета-клетки.
«Мы экспрессировали PMN в целом ряде тканей у одно-двухмесячных мышей», - говорит доктор Стэнджер. «Через три дня мыши умирали от гипогликемии».
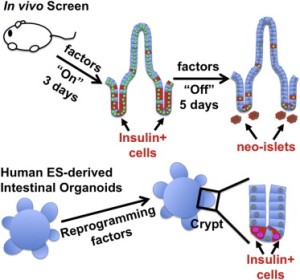
Взаимопревращение терминально дифференцированных клеток может служить мощным инструментом лечения дегенеративных заболеваний, включая диабет, на основе клеточной терапии. Чтобы определить, какие, если таковые существуют, взрослые ткани способны активировать программу островковых бета-клеток, ученые провели in vivo скрининг широкого спектра тканей путем экспрессии в них трех факторов перепрограммирования в бета-клетки. Они установили, что временная экспрессия этих факторов – Pdx1, MafA и Ngn3 (PMN) – в кишечнике способствует быстрой конверсии клеток кишечных крипт в эндокринные клетки, которые сливаются в «неоостровки» ниже основания крипт. Клетки неоостровков экспрессируют инсулин и демонстрируют ультраструктурные особенности бета-клеток. Важно отметить, что кишечные неостровки отвечают на глюкозу и в состоянии снижать гипергликемию у больных диабетом мышей. Кроме того, экспрессия PMN в человеческих кишечных «органоидах» стимулирует превращение эпителиальных клеток кишечника в бета-подобные клетки. Таким образом, эти результаты демонстрируют, что кишечник является доступным и обильным источником функциональных инсулин-продуцирующих клеток. (Рис. Cell Reports)
Исследователи поняли, что какие-то из мышиных клеток (не ацинарные) вырабатывали слишком много дополнительного инсулина, фактически летальное его количество.
Отследив, что это был за тип клеток, «мы увидели временную экспрессию этих трех факторов в клетках крипт кишечника около поджелудочной железы», объясняет доктор Стэнджер.
Ученые назвали эти бета-подобные трансформированные клетки «неоостровковыми». Неоостровковые клетки экспрессировали инсулин и демонстрировали структурные особенности бета-клеток. Кроме того, они реагировали на глюкозу: под ее воздействием они секретировали инсулин, а также устраняли гипергликемию у больных диабетом мышей.
Исследователи выяснили, как включить эти факторы только в клетках крипт кишечника с тем, чтобы не допустить побочного эффекта смертельной гипогликемии, убивавшей мышей.
Более того, экспрессия PMN в человеческой кишечных «органоидах» – миниатюрных кишечных структурных единицах, которые могут быть выращены в культуре, – также трансформирует кишечные эпителиальные клетки в бета-подобные клетки.
«Наши результаты показывают, что кишечник может быть доступным и богатым источником функциональных инсулин-продуцирующих клеток», - говорит доктор Стэнджер. «Наша конечная цель – получить эпителиальные клетки больных сахарным диабетом, которым проводилась эндоскопия, размножить эти клетки, ввести в них PMN, чтобы трансформировать их в бета-подобные клетки, а затем вернуть их пациенту в качестве заместительной терапии. Чтобы это стало возможным, предстоит пройти длинный путь: нужно, в том числе, улучшить функциональные свойства этих клеток так, чтобы они больше напоминали бета-клетки, и найти альтернативные способы трансформации клеток кишечника в бета-подобные клетки без генной терапии».
По материалам
Cellular Alchemy: Penn Study Shows How to Make Insulin-Producing Cells from Gut Cells
Оригинальная статья:
Yi-Ju Chen, Stacy R. Finkbeiner, Daniel Weinblatt, Matthew J. Emmett, Feven Tameire, Maryam Yousefi, Chenghua Yang, Rene Maehr, Qiao Zhou, Ruth Shemer, Yuval Dor, Changhong Li, Jason R. Spence, Ben Z. Stanger. De Novo Formation of Insulin-Producing "Neo-β Cell Islets" from Intestinal Crypts
© «Клеточная алхимия: инсулин-продуцирующие клетки можно получать из клеток кишечника». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Диабет.
Related Articles: |













