|
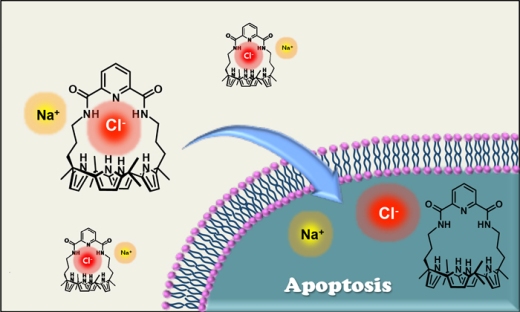
Синтетический переносчик ионов индуцирует апоптоз путем переноса в клетки хлоридного аниона. (Фото: University of Texas at Austin)
Ученые Техасского университета в Остине (University of Texas at Austin) и пяти других научных центров создали молекулу, вызывающую саморазрушение раковых клеток за счет переноса в них ионов натрия и хлора. Вновь созданный синтетический переносчик ионов, описанный в статье в журнале Nature Chemistry, подтверждает гипотезу, выдвинутую еще два десятилетия назад, предлагавшую новую стратегию разработки противоопухолевых препаратов и препаратов для лечения муковисцидоза.
Синтетические переносчики ионов разрабатывались и раньше, но их работу в реальной биологической системе, в которой перенесенные ионы очевидно вызывают саморазрушение клеток, ученым удалось показать впервые.
Чтобы поддерживать стабильную концентрацию ионов в своих мембранах, клеткам человеческого организма приходится «усердно трудиться». Нарушение этого хрупкого баланса может стать триггером апоптоза, или запрограммированной клеточной смерти, – механизма, используемого организмом для удаления поврежденных или опасных клеток.
Одним из путей уничтожения раковых клеток могло бы быть инициирование генетической программы самоуничтожения за счет перераспределения ионного баланса. К сожалению, раковое перерождение клетки приводит к блокированию в ней апоптоза, что объясняется изменением способа трансмембранного переноса ионов.
Почти два десятилетия назад было открыто природное химическое соединение продигиозин (prodigiosin), являющееся естественным переносчиком ионов и обладающее противораковым действием.

Профессор Колледжа естественных наук Техасского университета в Остине Джонатан Сесслер (Jonathan Sessler). (Фото: University of Texas at Austin)
С тех пор, по словам соавтора исследования профессора Колледжа естественных наук (College of Natural Sciences) Техасского университета в Остине Джонатана Сесслера (Jonathan Sessler), найти «синтетические переносчики, способные делать то же самое, но более эффективно, и обладающие свойством лечить такие заболевания, как муковисцидоз, при котором нарушается работа хлоридных каналов» стало «мечтой любого химика».
Профессор Сесслер и его коллеги во главе с профессорами Иньяэ Шином (Injae Shin) из Университета Йонсей (Yonsei University) и Филипом Гейлом (Philip Gale) из Университета Саутгемптона (University of Southampton) и Университета короля Абдулазиза (King Abdulaziz University) смогли воплотить эту мечту в жизнь.
Члены исследовательской группы, представлявшие Техасский университет, создали синтетический переносчик ионов, связывающийся с хлорид-ионами. Эта молекула работает за счет того, что окружает хлорид-ион органическим «одеялом», позволяющим ему растворяться в клеточной мембране, состоящей в основном из липидов, и имеет тенденцию использовать естественно присутствующие в клеточной мембране натриевые каналы, переносящие через мембрану ионы натрия.
Профессор Гейл и его коллеги установили, что этот переносчик эффективен в модельной системе искусственных липидных мембран.
Затем профессору Шину и его группе удалось показать, что эти молекулы способствуют гибели выращенных в культуре раковых клеток человека. Одним из ключевых выводов, к которым пришли исследователи, является тот, что концентрации ионов в раковых клетках изменяются до инициирования апоптоза, а не есть побочный эффект их гибели.
«Таким образом, мы замкнули цикл и показали, что поступление в клетку хлорид-ионов с помощью нашего синтетического переносчика действительно запускает апоптоз», - комментирует результаты работы профессор Сесслер. «Это очень интересно, потому что указывает на новый подход к созданию противоопухолевых препаратов».
На настоящий момент их синтетическая молекула вызывает запрограммированную смерть как раковых, так и здоровых клеток, уточняет ученый. Чтобы использовать переносчик анионов хлора для лечения рака, нужно разработать его вариант, связывающийся только с раковыми клетками. Это может быть сделано путем связывания переносчика с направляющей сайт-специфической молекулой, такой как молекула тексафирина (texaphyrin), уже синтезированной в лаборатории Сесслера.
Результаты этого исследования – кульминация многих лет работы шести университетов на трех континентах.
«Мы продемонстрировали, что этот механизм эффективен, что существовавшая более двух десятилетий идея научно обоснована, и это чрезвычайно интересно», - подводит итог профессор Сесслер. «Мы смогли показать, что и натрий и хлорид действительно поступают [в клетку]. Сейчас, я думаю, остается очень мало сомнений в применимости этой двухдесятилетней гипотезы».
Следующим шагом исследователей будет тестирование их синтетических переносчиков ионов на животных моделях.
По материалам
Synthetic Molecule Makes Cancer Self-Destruct
Оригинальная статья:
Sung-Kyun Ko, Sung Kuk Kim, Andrew Share, Vincent M. Lynch, Jinhong Park, Wan Namkung, Wim Van Rossom, Nathalie Busschaert, Philip A. Gale, Jonathan L. Sessler & Injae Shin. Synthetic ion transporters can induce apoptosis by facilitating chloride anion transport into cells
© «Синтетическая молекула вызывает апоптоз раковых клеток». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Нанотехнологии в медицине и биологии. Письменное разрешение обязательно.
Related Articles: |













