|
Человеческие нейральные клетки-предшественники, выделенные из развивающегося человеческого мозга и направленные по пути линейной дифференциации. Нейральные клетки-предшественники окрашены зеленым; дифференцированные астроциты – оранжевым; ядра – синим. (Фото: National Institute of Neurological Disorders and Stroke)
Ученые из Школы медицины Калифорнийского университета в Сан-Диего (University of California, San Diego School of Medicine) открыли новую функцию одного их известных белков. Он работает в биологической сети, определяя, останется ли незрелая нервная клетка в стволовом состоянии или трансформируется в функциональный нейрон.
Это открытие, опубликованное онлайн в журнале Cell Reports, более полно освещает фундаментальное, но все еще плохо изученное клеточное событие и может оказать значительное влияние на разработку в будущем новых методов лечения ряда неврологических заболеваний, включая аутизм и шизофрению.
Постдокторант Чи-Хун Лоу (Chih-Hong Lou), работая с профессором кафедры репродуктивной медицины Майлзом Вилкинсоном (Miles Wilkinson), PhD, научным сотрудником Института геномной медицины UC San Diego, и другими коллегами, установили, что это важнейшее биологическое решение контролируется белком UPF1, необходимым для пути нонсенс-опосредованного распада РНК (nonsense-mediated RNA decay, NMD).
Как ранее установлено, NMD играет две важные роли. Во-первых, это механизм контроля над качеством, используемый клетками для разрушения дефектных матричных РНК (мРНК) – молекул, необходимых для перевода генетической информации в белки. Во-вторых, он разрушает определенную группу нормальных мРНК. Как предполагалось, последняя функция NMD физиологически важна, но до сих пор оставалось неясным, выполняет ли ее NMD.
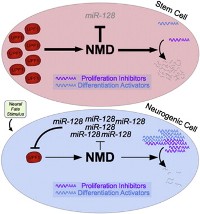
Профессор Вилкинсон и его коллеги установили, что во взаимодействии с классом РНК, называемых микроРНК, белок UPF1 действует как молекулярный переключатель, определяющий, когда незрелые (нефункциональные) нервные клетки дифференцируются в неделящиеся (функциональные) нейроны. В частности, UPF1 вызывает распад определенной матричной РНК, кодирующей белок сигнального пути TGF-β, стимулирующий нейральную дифференциации. Разрушение этой мРНК приводит к невозможности синтезировать кодируемый ею белок, что предотвращает нейральную дифференциацию. Таким образом, ученые впервые идентифицировали молекулярную сеть, в которой NMD действует в качестве драйвера нормальной биологической реакции.
Кроме того, нонсенс-опосредованный распад РНК способствует разрушению матричных РНК, кодирующих ингибиторы пролиферации, что, по мнению профессора Вилкинсона, может объяснить, почему NMD стимулирует пролиферативное состояние, характерное для стволовых клеток.
«Это открытие может иметь большое значение для клинической медицины», - считает профессор Вилкинсон. «Во-первых, за счет того, что NMD поддерживает стволовое состояние клеток, этот путь может оказаться полезным для более эффективного перепрограммирования дифференцированных клеток в стволовые. Еще одно применение следует из открытия того, что NMD жизненно важен для нормального развития мозга у самых разных видов, включая человека. У людей с нарушениями в NMD диагностируется умственная отсталость, а также, часто, шизофрения и аутизм. Методы лечения, направленные на устранение этих нарушений у пациентов, могут помочь в восстановлении правильного баланса стволовых клеток и дифференцированных нейронов и, тем самым, в восстановлении нормальной функции мозга».
По материалам
Protein Switch Dictates Cellular Fate: Stem Cell or Neuron
Оригинальная статья:
Chih H. Lou, Ada Shao, Eleen Y. Shum, Josh L. Espinoza, Lulu Huang, Rachid Karam, Miles F. Wilkinson. Posttranscriptional Control of the Stem Cell and Neurogenic Programs by the Nonsense-Mediated RNA Decay Pathway
Источник: NanoNewsNet
Related Articles: |













