|
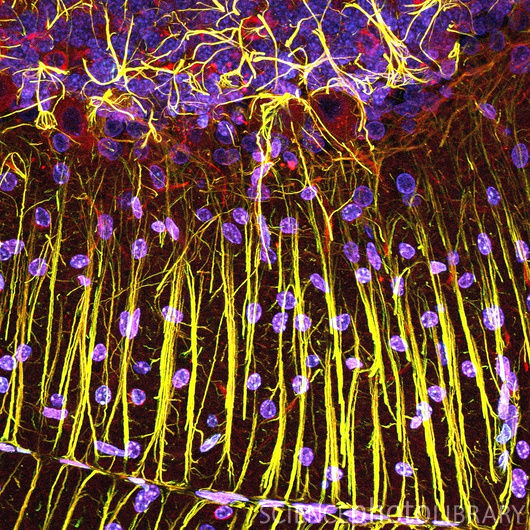
Срез ткани мозжечка. Клетки Пуркинье – тип нейронов – красные, клетки радиальной глии – желтые, клеточные ядра – фиолетовые. Грушевидные клетки Пуркинье имеют множество ветвящихся отростков (дендритов), получающих импульсы от других клеток и направляющихся к поверхности мозжечка. Клетки радиальной глии играют важнейшую роль в нейрональной миграции, построении слоев коры и мозжечка, а также являются клетками-предшественниками в процессе нейрогенеза. Радиальная глия образуется на ранней стадии развития нервной системы из нейроэпителиальных клеток. (Конфокальная световая микроскопия). (Фото: Science Photo Library/P360/0432)
Ученые всемирно известной Cold Spring Harbor Laboratory (CSHL) расшифровали одну из важнейших частей головоломки, давно не дающей покоя ученым-неврологам – как клетки-предшественники в развивающемся мозге млекопитающих воспроизводят самих себя и одновременно дают начало нейронам, заселяющим развивающуюся кору головного мозга.
Профессор CSHL Линда ван Эйлст (Linda Van Aelst), PhD, и ее коллеги поставили своей целью разгадать загадку, касающуюся клеток радиальной глии (radial glial cells, RGCs), являющихся предшественниками пирамидальных нейронов – наиболее распространенного типа возбуждающих нейронов в зрелой коре млекопитающих.
На генетически модифицированных мышах профессор ван Эйлст и сотрудники ее лаборатории доктора Ю-Тин Янг (Yu-Ting Yang) и Чиа-Линь Ван (Chia-Lin Wang) продемонстрировали, что центральную регуляторную роль в процессе, определяющем, как и когда клетки радиальной глии «решают» либо пролиферировать, то есть увеличить количество таких же, как они клеток-предшественников, либо дифференцироваться в клетки, которые впоследствии трансформируются в пирамидальные нейроны, играет белок DOCK7. Результаты исследования опубликованы в журнале Nature Neuroscience.
То, что в разных отделах развивающегося мозга грызунов, включая гиппокамп и кору, уровень экспрессии DOCK7 очень высок, уже было известно. Ранее ван Эйлст и ее коллеги показали, что этот белок контролирует образование аксонов.
Регуляторная роль белка DOCK7 была установлена в экспериментах, в которых его экспрессия либо подавлялась, либо усиливалась.
При подавлении DOCK7 в мышиных эмбрионах дифференцировка в нейроны затруднялась, и клетки радиальной глии оставались в своем прогениторном состоянии. При его гиперэкспрессии RGCs преждевременно дифференцировались, в результате чего нейронов становилось больше, а RGCs – меньше.
Эти и другие эксперименты выявили механизм, посредством которого экспрессия DOCK7 влияет на две жизненно важные, но противоположные функции клеток радиальной глии.
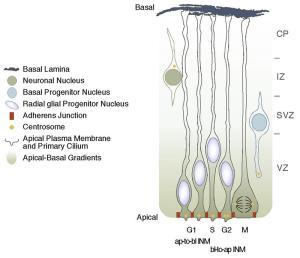
Белок DOCK7 регулирует миграцию клеток радиальной глии (RGCs) от базальной к апикальной поверхности вентрикулярной зоны (VZ) в развивающейся коре головного мозга мыши. На нижней (апикальной) поверхности VZ доминируют сигналы, направляющие RGCs к пролиферации, то есть к воспроизводству новых клеток радиальной глии. На верхней (базальной) поверхности VZ доминирующие сигналы заставляют RGCs дифференцироваться в новые промежуточные предшественники или нейроны. (Рис. Cold Spring Harbor Laboratory)
«Для правильного развития коры самовосстановление клеток радиальной глии и их дифференциация должны быть точно сбалансированы», - объясняет профессор ван Эйлст.
Открытый ими ключевой механизм определения судьбы клеток радиальной глии ученые назвали интеркинетической ядерной миграцией (interkinetic nuclear migration, или INM).
При интеркинетической ядерной миграции на протяжении клеточного цикла ядро клетки радиальной глии перемещается «вверх» и «вниз» между противоположными сторонами апикальной области нейроэпителия, называемой вентрикулярной зоной (ВЗ). Ядра движутся от апикальной поверхности во время фазы G1, проходят фазу S у базальной области ВЗ и возвращаются к апикальной поверхности в фазе G2, разделяясь у нее.
Белок DOCK7 регулирует это перемещение. В частности, ученые продемонстрировали миграцию ядер от базальной к апикальной области. У «нижней», апикальной, поверхности ВЗ доминируют сигналы, направляющие клетки радиальной глии к пролиферации – то есть воспроизводству RGCs. У «верхней», или базальной, области ВЗ доминирующие сигналы заставляют клетки радиальной глии дифференцироваться в новые промежуточные прогетиторы или нейроны.
«Клеточный механизм, управляющий интеркинетической ядерной миграцией, включает в себя белковый комплекс актина и миозина, называемый актомиозином, а также систему, зависимую от микротрубочек», - поясняет доктор Ван. «Мы показали, как DOCK7 осуществляет свои функции, противодействуя функции белка TACC3, стимулирующего рост микротрубочек». Что характерно, этот белок связан с центросомой – клеточной органеллой, организующей микротрубочки, – и регулирует рост микротрубочек, исходящих от центросомы, связывая, таким образом, центросому и ядро.
DOCK7 является антагонистом белка TACC3, стимулирующего рост микротрубочек. Сайленсинг DOCK7 усиливает движение ядер клеток радиальной глии от базальной к апикальной области ВЗ, приводя к их накоплению в этой области, а апикальные митозы увеличивают количество RGCs и уменьшают количество нейронов. В противоположность этому, гиперэкспрессия DOCK7 приводит к накоплению ядер у базальной поверхности и митозам вдалеке от апикальной поверхности, где за счет пролиферации большего количества предшественников усиливается образование новых нейронов, отмечает доктор Ян.
Помимо открытия важного механизма развития коры новое исследование может пролить свет на патологию, наблюдаемую при микроцефалии - заболевании, характеризующемся аномально малыми размерами мозга, а также на нарушения развития нервной системы, такие как шизофрения.
«При аномальной экспрессии DOCK7 нарушается нормальный нейрогенез», - говорит ван Эйлст. «В будущем мы надеемся выяснить, связан ли дисбаланс в нейрогенезе, вызванный аберрациями DOCK7, с последующим дисбалансом в кортикальных нервных сетях и различными известными патологиями».
По материалам
Research identifies protein that regulates key ‘fate’ decision in cortical progenitor cells
Оригинальная статья:
Yu-Ting Yang, Chia-Lin Wang, Linda Van Aelst. DOCK7 interacts with TACC3 to regulate interkinetic nuclear migration and cortical neurogenesis
© «Найден белок, определяющий судьбу клеток радиальной глии». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Стволовые клетки. Письменное разрешение обязательно
Еще о радиальной глии
В спинном мозге обнаружены клетки радиальной глии с функцией нейральных стволовых клеток
и о стволовых клетках
От эмбриональной стволовой клетки до кардиомиоцита: составлена геномная карта сердца
Перепрограммирование клеток: идентифицированы новые маркеры плюрипотентности
Открытие сигнатуры перепрограммирования поможет устранить препятствия в использовании стволовых клеток в регенеративной медицине
Установлено значительное сходство индуцированных плюрипотентных стволовых и раковых клеток
Ученые остановили возрастную потерю мышечной массы у мышей
Найден ключ к восполнению возрастной потери мышечной массы
Рак и старение связаны дисфункцией стволовых клеток
Субпопуляция макрофагов поддерживает молодость кроветворных стволовых клеток
Раковые стволовые клетки неохотно специализируются в низкокислородной среде
Из индуцированных плюрипотентных стволовых клеток получена хрящевая ткань
Related Articles: |













