|

Профессор кафедры сравнительных биологических наук Сюзанна Берри-Миллер (Suzanne Berry-Miller), профессор кафедры ветеринарной клинической медицины Роберт О’Брайен (Robert O’Brien) Университета штата Иллинойс и их коллеги разработали метод усиления сердечной функции в мышиной модели мышечной дистрофии Дюшенна. (Фото: L. Brian Stauffer)
Пересадка стволовых клеток, полученных из нормальных кровеносных сосудов мышей, в сердце животных с модель мышечной дистрофии Дюшенна (МДД) предотвращает ослабление сердечной функции, вызванное этим заболеванием.
Мышечная дистрофия Дюшенна – генетическое заболевание, вызванное мутацией в гене дистрофина – белка, без которого мышечные сокращения разрывают клеточные мембраны, приводя к гибели клеток. Потерянные клетки могут быть восстановлены, но со временем их замещает рубцовая ткань – причина мышечной слабости и проблем с сердцем, типичных для МДД.
По оценкам Центров профилактики и контроля над заболеваниями США (U.S. Centers for Disease Control and Prevention), мышечная дистрофия Дюшенна поражает одного из каждых 3500 мальчиков. Болезнь чаще встречается у мужчин, так как ген дистрофина находится в Х-хромосоме. У мужчин одна Х- и одна Y-хромосома, поэтому мужчины с мутацией в этом гене подвержены заболеванию. У женщин две Х-хромосомы, и для развития МДД необходимо, чтобы мутация присутствовала в обеих хромосомах. Но у женщин с мутацией в одной хромосоме иногда тоже развивается мышечная слабость и наблюдаются проблемы с сердцем. Кроме того, они могут передавать эту мутацию своим детям.
Несмотря на то, что успехи медицины позволили увеличить продолжительность жизни пациентов с МДД до 30 с небольшим лет, обусловленное болезнью повреждение сердца и диафрагмы, по-прежнему, ограничивает ее. Почти у 100 процентов пациентов развивается дилатационная кардиомиопатия, при которой ослабленное сердце с увеличенными камерами препятствует нормальному обеспечению организма кровью.
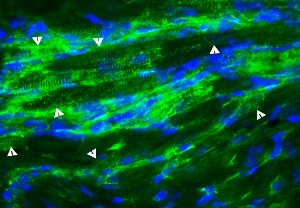
Введение стволовых клеток, полученных из кровеносных сосудов, стимулирует образование новых кардиомиоцитов (показаны стрелками) уже присутствующими в сердце нестин-положительными стволовыми клетками. (Фото: Suzanne Berry-Miller)
«Сегодня врачи воздействуют на симптомы этого сердечного заболевания, назначая пациентам препараты, способствующие продлению функции сердца, но это не может заменить утраченные или поврежденные клетки», - говорит профессор кафедры сравнительных биологических наук Университета Иллинойса (University of Illinois) Сюзанна Берри-Миллер (Suzanne Berry-Miller), возглавлявшая исследование.
Профессор Берри–Миллер и ее коллеги инъецировали в сердце дистрофин-дефицитных мышей – модели мышечной дистрофии Дюшенна человека – стволовые клетки, известные как аортопроизводные мезоангиобласты (aorta-derived mesoangioblasts, ADM), с функциональной копией гена дистрофина.
Терапия стволовыми клетками предотвращала или отсрочивала проблемы с сердцем у мышей, у которых еще не наблюдалось признаков функциональных или структурных дефектов, типичных для мышечной дистрофии Дюшенна.
Пока профессор Берри-Миллер и ее коллеги не знают причин улучшения функции сердца, но видят три возможных механизма. Они наблюдали, что некоторые из введенных стволовых клеток стали новыми клетками сердечной мышцы, экспрессирующими отсутствующий дифстрофин. Кроме того, лечение заставило делиться и стать новыми кардиомиоцитами существующие стволовые клетки сердца. Стволовые клетки стимулировали образование в сердце новых кровеносных сосудов. По словам Берри-Миллер, еще не ясно, какой из этих эффектов ответственен за задержку развития кардиомиопатии.
«Эти производные сосудистых клеток могут быть хорошими кандидатами для терапии, но более важно то, что наши результаты дают новые потенциальные терапевтические мишени для изучения, которые можно активировать напрямую, без введения клеток, таких как ADM в данном исследовании, в организм пациента», - комментирует результаты экспериментов профессор Берри-Миллер. «Активация уже присутствующих в организме стволовых клеток для восстановления тканей позволит исключить необходимость подбора совместимых доноров и избежать потенциального отторжения этих стволовых клеток организмом пациента».
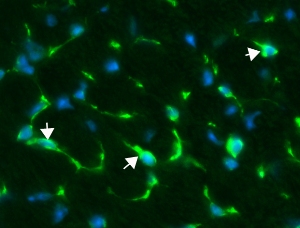
После введения в сердце дистрофин-дефицитных мышей стволовых клеток, полученных из нормальных кровеносных сосудов, ученые наблюдали усиление клеточного деления нестин-позитивных стволовых клеток (показаны зеленым). Эти стволовые клетки присутствуют в сердце взрослых организмов – человека, крыс и мышей, но их функция пока неизвестна. Кроме того, было установлено и усиление образования из нестин-позитивных стволовых клеток новых клеток сердечной мышцы. (Фото: Suzanne Berry-Miller)
Несмотря на обнадеживающие результаты, показывающие пользу от введения стволовых клеток до возникновения патологии, у мышей с уже развившейся дилатационной кардиомиопатией, одной из характеристик которой является замещение мышц соединительной тканью, известное как фиброз, отмечалось дальнейшее ослабление функции сердца.
По мнению профессора Берри-Миллер, это может быть результатом того, что стволовые клетки попадают не в мышечную ткань, а в фиброзный карман. В этом случае они могут стать фибробластами, образующими еще большее количество соединительной ткани, усиливая рубцевание и еще более ослабляя функцию сердца. Это говорит о том, что важную роль в усилении функции сердца у мышей, не экспрессирующих дистрофин, играют сроки введения стволовых клеток.
Профессор Берри-Миллер уверена, что полученные результаты являются трамплином к новым клиническим мишеням для лечения пациентов с мышечной дистрофией Дюшенна.
«На сегодняшний день это единственное исследование, в котором в результате введения стволовых клеток наблюдалось улучшение функции дистрофин-дефицитного сердца и образование из эндогенных стволовых клеток новых мышечных клеток, заместивших потерянные. Я думаю, оно открывает новые области, на которых нужно сосредоточить внимание, в доклинических исследованиях методов лечения МДД», - заключает ученый.
Результаты исследования опубликованы в журнале Stem Cells Translational Medicine.
По материалам
Stem-cell approach shows promise for Duchenne muscular dystrophy
Оригинальная статья:
Ju Lan Chun, Robert O'Brien, Min Ho Song, Blake F. Wondrasch and Suzanne E. Berry. Injection of vessel derived stem cells-prevent dilatedcardiomyopathy and promote angiogenesis and endogenous cardiac stem cell proliferation in mdx/utrn-/-but not aged mdx mouse models for Duchenne muscular dystrophy
© «Лечение мышечной дистрофии Дюшенна стволовыми клетками может оказаться перспективным подходом». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Стволовые клетки. Письменное разрешение обязательно.
Еще о стволовых клетках
Судьбу раковых стволовых клеток решает протеинкиназа Akt
Новое о роли эпигенетики в судьбе стволовых и раковых клеток
Трансплантация нейральных стволовых клеток замедляет прогрессию бокового амиотрофического склероза у мышей
Разработан более быстрый и безопасный метод получение стволовых клеток
Ретровирус в геноме человека активен в плюрипотентных стволовых клетках
Судьба эмбриональной стволовой клетки: ученые раскрывают эпигенетические механизмы плюрипотентности и дифференциации ЭСК
Определена молекула, противодействующая старению кожи
Перепрограммирование клеток: определена структура важнейшего элемента белка Oct4
Найдена молекула-триггер, направляющая дифференциацию стволовых клеток скелетных мышц
Немецкие ученые нашли причину возрастного снижения когнитивных способностей
Related Articles: |













