|
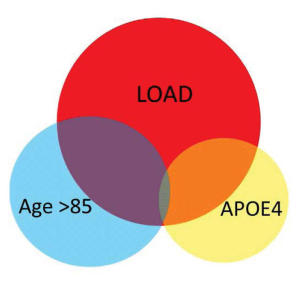
Перекрывание изменений в экспрессии генов мозга здоровых лиц, несущих вариант высокого риска APOE4, здоровых людей в возрасте старше 85 лет и пациентов с болезнью Альцгеймера с поздним началом (LOAD). (Фото: Dr. Asa Abeliovich, Columbia University's Taub Institute)
Предложены новые гены-мишени для лечения болезни Альцгеймера
Ученые Медицинского центра Колумбийского университета (Columbia University Medical Center, CUMC) идентифицировали ключевой молекулярный путь, приводящий в конечном итоге к болезни Альцгеймера с поздним началом – наиболее распространенной форме заболевания. Новое исследование представляет на суд научного сообщества новый подход к пониманию болезни Альцгеймера и предлагает несколько новых потенциальных мишеней лекарственных препаратов. Работа опубликована в журнале Nature.
Многое из того, что известно о болезни Альцгеймера, имеет своим источником лабораторные исследования редких наследственных форм этого заболевания с ранним началом.
«Такие исследования дали в руки ученых важные ключи к процессам, лежащим в основе этого заболевания, но как эти редкие семейные формы болезни Альцгеймера связаны с самой распространенной его формой, остается неясным», - говорит руководитель исследования Аса Абелиович (Asa Abeliovich), MD, PhD, адъюнкт-профессор патологии & клеточной биологии и неврологии Научно-исследовательского института болезни Альцгеймера и старения мозга Тауба (Taub Institute for Research on Alzheimer's Disease and the Aging Brain) CUMC. «Самое важное, десятки препаратов, «работающих» на мышиных моделях семейной формы заболевания, в конечном счете, терпят неудачу в испытаниях на пациентах с болезнью Альцгеймера с поздним началом. Это заставило нас, и другие лаборатории, искать механизмы распространенной формы заболевания».
Несемейная форма болезни Альцгеймера очень сложна. Считается, что в ее основе лежит сочетание генетических и экологических факторов риска, эффект каждого из которых по отдельности довольно незначителен. В предшествующих работах с использованием так называемого общегеномного исследования ассоциаций (genome-wide association studies, GWAS) было выявлено несколько общих генетических вариантов, повышающих вероятность развития болезни Альцгеймера. Ключевая цель ученых состоит в том, чтобы понять, как именно эти общие генетические варианты влияют на риск развития заболевания.
Ученым CUMC удалось определить ключевые молекулярные пути, связывающие генетические факторы риска с болезнью Альцгеймера. В их работе методы клеточной биологии сочетались с инструментами системной биологии – в данном случае с вычислительным анализом сложной сети изменений в экспрессии генов клеток человеческого мозга, подверженного риску развития заболевания.
В частности, исследователи сосредоточили свое внимание на одном из наиболее значимых генетических факторов, ассоциируемых с высоким риском развития болезни Альцгеймера, – гену APOE4 (присутствующему в геноме примерно трети всей человеческой популяции). Одна копия этого генетического варианта повышает риск развития болезни Альцгеймера с поздним началом в три раза, в то время как две копии – в десять раз.
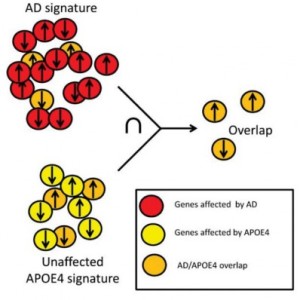
Схема перекрывающихся изменений в экспрессию генов, наблюдаемых в здоровой ткани мозга у лиц с высоким риском развития болезни Альцгеймера и при развившемся заболевании. (Фото: Dr. Asa Abeliovich, Columbia University's Taub Institute)
«В этом исследовании, - говорит доктор Абелиович, - мы поставили вопрос так: наблюдается ли постоянная картина в аутопсийных образцах мозговой ткани лиц с высоким риском развития болезни Альцгеймера?».
Удивительно, но даже при отсутствии болезни Альцгеймера в ткани головного мозга лиц с высоким риском (несущих в своих генах APOE4) наблюдались определенные изменения, свойственные клинически проявленному заболеванию. Поэтому ученые сфокусировались на попытках понять эти, по-видимому, подвергающие человека риску изменения. Их эксперименты были основаны на транскриптомике – широкомасштабном обзоре уровня активности тысяч экспрессирующихся в мозге генов.
Используя упомянутые выше инструменты сетевого анализа, исследователи идентифицировали около десятка кандидатов на роль «главных регуляторов», связывающих APOE4 с каскадом разрушительных событий, кульминацией которых является деменция. Последующие эксперименты на клетках показали, что некоторые из этих главных регуляторов участвуют в процессинге и трафике белка-предшественника амилоида (amyloid precursor protein, APP) в нейронах головного мозга. Белок-предшественник амилоида дает начало бета-амилоиду - белку, накапливающемуся в клетках мозга пациентов с болезнью Альцгеймера. В конечном итоге, работа связывает общий генетический фактор, связанный с высоким риском развития болезни Альцгеймера, APOE4 и патологию заболевания.
Из выявленных вероятных «главных регуляторов» особое внимание ученые уделили анализу двух генов – SV2A и RFN219.
«Нас особенно заинтересовал SV2A – мишень часто назначаемого противоэпилептического препарата леветирацетама [levetiracetam]. Это предполагает терапевтическую стратегию. Но, прежде чем мы сможем разработать клинические испытания леветирацетама на пациентах с симптомами болезни Альцгеймера с поздним началом, необходимо провести дополнительные исследования», - говорит доктор Абелиович.
Ученые оценили роль SV2A, используя человеческие индуцированные нейроны, несущие генетический вариант APOE4. Эти нейроны были получены путем прямого перепрограммирования фибробластов кожи лиц с высоким риском развития болезни Альцгеймера с помощью методики, разработанной в лаборатории доктора Абелиовича. Обработка нейронов, несущих фактор риска APOE4, леветирацетамом, ингибирующим SV2A, приводила к снижению образования бета-амилоида. Кроме того, исследование выявило роль гена RFN219, который в клетках с вариантом АРОЕ4, по-видимому, играет определенную роль в процессинге APP.
«Наши результаты говорят о том, что как SV2A, так и RFN219 являются вероятными мишенями лекарственных препаратов», - подводит итог доктор Абелиович. «Эти подходы могут сыграть определенную роль в разработке препаратов для лечения распространенной несемейной формы болезни Альцгеймера, что представляет особый интерес, так как остается огромной проблемой».
По материалам
Key Molecular Pathways Leading to Alzheimer’s Identified
Оригинальная статья:
Herve Rhinn, Ryousuke Fujita, Liang Qiang, Rong Cheng, Joseph H. Lee, Asa Abeliovich. Integrative genomics identifies APOE ε4 effectors in Alzheimer's disease
© «Определен ключевой молекулярный путь, ведущий к развитию болезни Альцгеймера». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Болезнь Альцгеймера.
Related Articles: |













