|
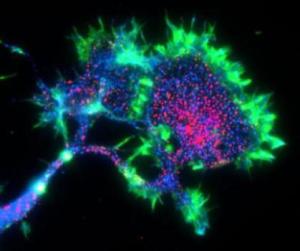
PirB (красный) сконцентрирован на поверхности растущих нервных клеток. (Фото: Dr. Carla Shatz, Stanford University)
Ученые из Школы медицины Стэнфордского университета (Stanford University School of Medicine) в сотрудничестве со своими коллегами из Гарвардского университета (Harvard University) показали, как бета-амилоид, вовлеченный в развитие болезни Альцгеймера, разрушает синапсы задолго до образования бляшек, приводящих к смерти нервных клеток.
Ключевыми особенностями болезни Альцгеймера, которой только в США страдает около 5 миллионов человек, являются потеря синапсов – точек контакта между нейронами, посредством которых происходит передача электрохимических сигналов, – и параллельное нарушение функций мозга, в частности, снижение способности к запоминанию.
«Наше открытие показывает, что болезнь Альцгеймера начинает проявляться задолго до того, когда становится очевидным образование бляшек», - говорит руководитель исследования, опубликованного в журнале Science, Карла Шац, (Carla Shatz), PhD, профессор нейробиологии и биологии.
Результаты исследования, проведенного на мышах и тканях человеческого мозга, возможно, помогут объяснить неудачи проведенных за последние годы крупномасштабных клинических испытаний нескольких препаратов, целью применения которых было замедление прогрессирования болезни Альцгеймера, а мишенью – уже образовавшиеся в межнейронном пространстве бета-амилоидные бляшки. Кроме того, они могут указать путь к более эффективным методам лечения этого нейродегенеративного заболевания на его ранних стадиях.
Бета-амилоид начинает жизнь как одиночная молекула, имеющая тенденцию к образованию скоплений – сначала небольших все еще растворимых кластеров, способных свободно перемещаться по головному мозгу, а в конечном итоге бляшек, считающихся признаком болезни Альцгеймера. Профессор Шац и ее коллеги впервые показали, что в кластерной форме бета-амилоид может прочно связываться с рецептором на нервных клетках, запуская межклеточной процесс, нарушающий их связь с другими нейронами.
Нейроны связаны синапсами, и относительная сила межсинаптических связей может изменяться в ответ на новый опыт.
Используя экспериментальную линию мышей, предрасположенных к синаптическим и когнитивным нарушениям, характерным для болезни Альцгеймера, профессор Шац и ее коллеги показали, что, если у таких мышей нет поверхностного белка, обычно расположенного очень близко к синапсам, они проявляют устойчивость к потере памяти и синапсов, характерной для данного заболевания. Исследование показало, что этот белок – PirB (paired immunoglobulin-like receptor B), – является высокоаффинным рецептором бета-амилоида в его растворимой кластерной форме, что означает, что растворимые кластеры бета-амилоида очень прочно связываются с PirB. Это взаимодействие запускает каскад биохимических событий, кульминацией которого является разрушение синапсов.
Профессор Шац занималась изучением PirB в течение многих лет, но в другом контексте. На генетически модифицированных мышах, не имеющих этого белка, она изучала роль PirB в мозге. Ранее считалось, что PirB используется только клетками иммунной системы, но Шац установила, что он находится и на нервных клетках головного мозга, где подавляет способность синапсов усиливать свою функцию пропорционально степени их активности и фактически способствует их ослаблению. Присутствие в мозге таких тормозов желательно, потому что слишком лабильное изменение силы синапсов может привести к неблагоприятным последствиям, например, к эпилепсии.
В новом исследовании Шац и ее коллеги использовали другую линию генно-инженерных мышей, геном которых содержал мутантные копии двух генов человека. Известно, что каждая из этих двух мутаций делает организм человека предрасположенным к развитию болезни Альцгеймера. Присутствие обеих мутаций в геноме мышей, у которых никогда не развиваются амилоидные бляшки, с возрастом приводит к их выраженному образованию, а также последующему ухудшению результатов, демонстрируемых животными в различных тестах на память.

Карла Шац (Carla Shatz) – руководитель исследования, результаты которого говорят о том, что болезнь Альцгеймера начинается задолго до образования бляшек, вызывающих гибель нервных клеток. (Фото: Dr. Carla Shatz, Stanford University)
«Мне всегда казалось странным, что у этих мышей - и, по сути, у всех изучаемых нами и другими учеными мышиных моделей болезни Альцгеймера, - до старости нет никаких проблем с памятью», - говорит профессор Шац. «Ведь в мозге этих мышей высокие уровни бета-амилоида наблюдаются с очень раннего возраста».
Шац заинтересовало, нельзя ли найти более чувствительный показатель ранних эффектов бета-амилоида на молодой мозг. Исследование 2012 года показало, что в специфической области мозга молодых предрасположенных к болезни Альцгеймера мышей, синапсы которой у здоровых животных довольно пластичны в изменении их относительной силы, такой пластичности не наблюдается. Это предполагает, что трудно выявляемые эффекты болезни Альцгеймера развиваются гораздо раньше, чем бляшки или признаки потери памяти.
Ученые решили выяснить, может ли удаление PirB из генома мышей с моделью болезни Альцгеймера восстановить синаптическую пластичность. Они скрестили линию мышей, несущих гены болезни Альцгеймера, с линией с отсутствием белка PirB, создав гибриды. Эксперименты показали, что мозг молодых мышей с болезнью Альцгеймера, в котором отсутствовал PirB, сохранил такую же гибкость изменения синаптической силы, что и мозг нормальных мышей. Кроме того, мыши зрелого возраста с болезнью Альцгеймера, не имевшие PirB, показывали такие же результаты в тестах на память, что и нормальные мыши. При этом их ровесники – практически генетически идентичные и отличающиеся только способностью к экспрессии PirB – страдали выраженной потерей синапсов и памяти.
«Мыши с моделью болезни Альцгеймера без PirB были защищены от последствий мутаций, являющихся причиной образования бета-амилоида», - комментирует Шац.
Теперь перед учеными встал вопрос, почему?
Таехо Ким (Taeho Kim), PhD, постдокторант лаборатории Шац и ведущий автор статьи в Science, выдвинул гипотезу: может быть, PirB и бета-амилоид взаимодействуют? Это может заставить PirB «нажимать на тормоза» даже сильнее, чем обычно, ослабляя синапсы вплоть до их полного исчезновения. Дальнейшие эксперименты подтвердили, что бета-амилоид прочно связывается с PirB.
PirB – специфически мышиный белок, но доктор Ким открыл аналог этого бета-амилоидного рецептора в мозге человека – белок LilrB2 (leukocyte immunoglobulin-like receptor B2).
В другом эксперименте доктор Ким сравнил белки в мозге мышей с болезнью Альцгеймера с отсутствием PirB с белками животных с болезнью Альцгеймера, экспрессирующих этот белок. Последние показали значительное повышение активности со стороны нескольких белков, в частности, фермента кофилина (cofilin). В последующих исследованиях было установлено, что активность кофилина в посмертных образцах мозга пациентов с болезнью Альцгеймера также существенно выше, чем в мозге людей, не страдавших этим заболеванием.
Кофилин разрушает актин - белок, необходимый для поддержания структуры синапсов. И, как также показало новое исследование, связывание бета-амилоида с PirB приводит к биохимическим изменениям в кофилине, что повышает его разрушающую актин и синапсы активность.
«Нет актина, нет синапса», - поясняет Шац.
Гипотеза доктора Кима, по-видимому, верна. Бета-амилоид связывается с PirB (и, как доказали исследователи, с его человеческим аналогом – LilrB2), повышая активность кофилина и разрушая структурную целостность синапсов.
Хотя вполне могут существовать и другие магистральные пути разрушения синапсов, по мнению профессора Шац, их не может быть очень много. Она считает, что прямое участие бета-амилоида – а также кофилина, настолько очевидно вовлеченного в разрушение синапсов, – предполагает большое значение именно этого пути.
Она рассчитывает, что препараты, блокирующие связывание бета-амилоида с PirB на поверхности нервных клеток – например, растворимые фрагменты PirB, содержащие части этой молекулы, которые могли бы выступать в качестве «приманки» – будут обладать терапевтическим действием.
«Я надеюсь, что это открытие окажется достаточно интересным для фармацевтических и биотехнологических компаний, чтобы кто-то попытался продвинуть эту идею», - заключает ученый.
По материалам
Scientists reveal how beta-amyloid may cause Alzheimer's
Оригинальная статья:
Kim T, Vidal GS, Djurisic M, William CM, Birnbaum ME, Garcia KC, Hyman BT, and Shatz CJ. Human LilrB2 is a beta-amyloid receptor and its murine homolog PirB regulates synaptic plasticity in an Alzheimer's model
© «Как бета-амилоид разрушает синапсы». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Болезнь Альцгеймера.
Related Articles: |













