Перспективный подход к замедлению нейродегенерации при болезни Хантингтона

(thedubinclinic.com)
Исследование, представленное Линн Реймонд (Lynn Raymond), MD, PhD, из Университета Британской Колумбии (University of British Columbia), показывает, что блокирование определенного класса рецепторов глутамата, называемых внесинаптическими NMDA-рецепторами, может улучшить координацию движений и предотвратить гибель нервных клеток у животных с моделями болезни Хантингтона. Так как болезнь Хантингтона – наследственное заболевание – диагностируется за несколько десятилетий до появления клиники, более глубокое понимание самых ранних изменений в функциях клеток мозга и лежащих в основе этих изменений молекулярных путей может привести к разработке методов профилактики, способных отсрочить появление симптомов и нейродегенерацию.
Результаты, полученные группой доктора Реймонд, были представлены на Canadian Neuroscience Meeting 2014, 8-й ежегодной конференции Канадской ассоциации нейробиологов (Canadian Association for Neuroscience – Association Canadienne des Neurosciences (CAN-ACN)).

Невролог из Университета Британской Колумбии Линн Рэймонд (Lynn Raymond) изучает влияние препарата Мемантин на мышей с симптомами болезни Хантингтона. (Фото: University of British Columbia)
Глутамат давно признан нейромедиатором, способствующим гибели клеток, и его токсические эффекты опосредствуются семейством рецепторов, известных как NMDARs (N-метил-D-аспартат рецепторы глутамата). К сожалению, лечение заболеваний нервной системы путем блокирования NMDARs не приносит успеха, так как сопровождается многочисленными побочными эффектами. Недавняя гипотеза, основанная на результатах исследований целого ряда ученых, говорит о том, что NMDARs, расположенные в различных областях поверхности нейронов, могут производить противоположный эффект, чем можно объяснить, почему блокирование всех NMDARs – далеко не лучший вариант лечения. Синапсы являются структурой, связывающей нейроны и передающей между ними электрические или химические сигналы. Они несут рецепторы многих нейротрансмиттеров, так как это основное место передачи сигналов. Однако рецепторы есть и за пределами синапса, и в этом случае они называются внесинаптическими. Ряд недавних исследований показал, что функция NMDARs, расположенных в синапсах, заключается в усилении сигналинга выживаемости и стимуляции процессов обучения и памяти, в то время как внесинаптические NMDARs подавляют сигналинг выживания, препятствуют нормальной работе механизмов обучения и повышают активность путей, опосредующих апоптоз (запрограммированную клеточную смерть).
Используя препарат, избирательно блокирующий внесинаптические NMDARs (Мемантин), доктор Реймонд и ее коллеги смогли отсрочить проявление симптомов болезни Хантингтона в мышиной модели заболевания.
У мышей, пивших воду, содержавшую лекарственное средство, даже всего в течение двух месяцев до проявления симптомов заболевания, лучше вырабатывались моторные навыки и наблюдалась лучшая координация движений.
«Низкая доза лекарственного средства преимущественно просто блокирует внесинаптические рецепторы, оставляя необходимые для обучения и памяти нетронутыми», - комментирует эти результаты доктор Реймонд.
Однако в экспериментах на мышах исследователи наблюдали очень большую зависимость эффекта Мемантина от дозы: низкие дозы оказывали положительное воздействие, а их повышение сопровождалось блокированием всех NMDA-рецепторов. Это создает угрозу усугубить состояние, тем более что пока не совсем ясно, где пролегает этот рубеж.
Хотя на мышах Мемантин показал очень перспективные результаты, прежде чем этот препарат можно будет назначать пациентам с болезнью Хантингтона, необходимо провести его клинические испытания.
«Препарат¸ который мы использовали, – Мемантин – в настоящее время назначается пациентам с умеренно выраженными симптомами болезни Альцгеймера. Наши результаты показывают, что клинические испытания Мемантина и препаратов с аналогичным механизмом действия при болезни Хантингтона, особенно на доклинической стадии, полностью обоснованы», - продолжает Реймонд.
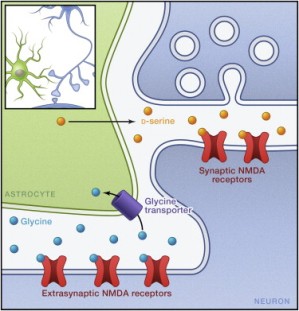
Синаптические и внесинаптические NMDA-рецепторы используют разные коагонисты. NMDA-рецепторы занимают уникальное место среди рецепторов нейротрансмиттеров, так как их активация требует связывания как с глутаматом, так и с коагонистом. Первоначально этим коагонистом считался глицин, хотя в последнее десятилетие стало ясно, что, во многих областях мозга, синаптические NMDA-рецепторы в качестве коагониста используют D-серин, высвобождаемый синапс-обволакивающими астроцитами. NMDA-рецепторы находятся и на внесинаптических мембранах, хотя физиологическая роль этих рецепторов пока почти непонятна. Как было показано в последние годы, основным коагонистом у внесинаптических NMDA-рецепторов является глицин, преимущественно выводимый из синапсов перисинаптическими переносчиками глицина. (Рис. Cell)
Пилотное исследование эффектов Мемантина на пациентах с уже развившимися симптомами болезни Хантингтона, помощь в проведении которого оказывала Реймонд, недавно завершено, но его результаты еще анализируются.
Доктор Реймонд надеется, что результаты этих тестов позволят перейти к клиническим испытаниям на пациентах, у которых присутствие ответственного на развитие болезни Хантингтона гена подтверждено генетическими исследованиями, но у которых еще не проявляются клинические симптомы заболевания.
Однако, скорее всего, это случится нескоро.
«Одной из проблем здесь является то, что [регулирующие органы системы здравоохранения] обеспокоены проведением испытаний на клинически здоровых людях», - объясняет она. «Это то, чего нам приходится добиваться с большим трудом».
Как известно, внесинаптические NMDARs вовлечены в развитие и других нейродегенеративных заболеваний, таких как болезнь Альцгеймера, а также последствий черепно-мозговых травм и некоторых форм инсульта. Поэтому полученные канадской группой результаты предполагают разработку новых путей лечения многих заболеваний, для которых характерны деградация и гибель нейронов, новых способов защиты нейронов до появления симптомов нейродегенерации.
По материалам
Promising approach to slow brain degeneration in a model of Huntington’s disease uncovered
© «Перспективный подход к замедлению нейродегенерации при болезни Хантингтона». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Болезнь Хантингтона. Письменное разрешение обязательно.
Related Articles: |













