|
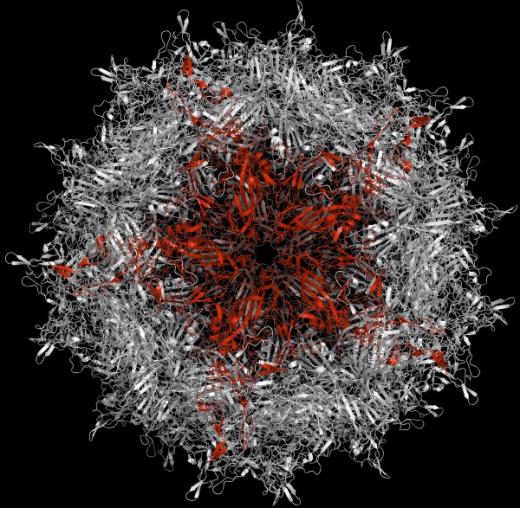
Модель аденоассоциированного вируса типа 2. (Фото: William Ray)
Вдохновленные успехами в коррекции наследственных форм слепоты, достигнутыми с помощью генной терапии, ученые из Школы медицины Перельмана (Perelman School of Medicine) Пенсильванского университета (University of Pennsylvania, Penn), намерены расширить сферу применения своего подхода на другие типы нарушений зрения.
В предыдущем исследовании, проведенном в Детской больнице Филадельфии (The Children's Hospital of Philadelphia) и Пенсильванском университете, ученые упаковали в генно-инженерный вектор – аденоассоциированный вирус (adeno-associated virus, AAV) – нормальный вариант гена, отсутствующего при врожденной дегенерации сетчатки Лебера (врожденном амаврозе Лебера). Врожденный амавроз Лебера – наследственная патология сетчатки, характеризующаяся слепотой с рождения или приводящая к слепоте в первые годы жизни, причиной чему является дегенерация фоторецепторных клеток. Вирусный вектор доставил ген в клетки сетчатки, туда, где он вырабатывает фермент, восстанавливающий фоторецепторы.
В настоящем исследовании, опубликованном в Science Translational Medicine, ученые сравнили на животной модели безопасность и эффективность двух различных серотипов AAV – AAV2, уже использованного в предыдущих испытаниях, и AAV8, представляющего AAV-технологию второго поколения. AAV8 впервые был выделен профессором кафедры патологии и лабораторной медицины Penn Джеймсом Вилсоном, MD, PhD. (James M. Wilson), соведущим автором статьи в STM.
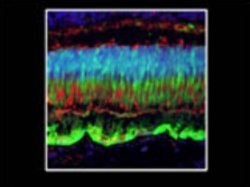
Зеленый флуоресцентный белок в фоторецепторных и пигментных эпителиальных клетках после субретинального введения вектора серотипа AAV8 в сетчатку обезьян. Ядра клеток помечены синим, фоторецепторы-палочки – красным цветом. (Фото: Luk Vandenberghe, PhD, Perelman School of Medicine at the University of Pennsylvania)
Оба вирусных вектора были использованы для доставки трансгена зеленого флуоресцентного белка (GFP) в пигментные эпителиальные (retinal pigment epithelial, RPE) клетки и клетки фоторецепторов сетчатки обезьян, не принадлежащих к высшим приматам – человекообразным обезьянам. Фоторецепторные клетки – проблемная область для многих заболеваний сетчатки, например, для наследственного пигментного ретинита, методов лечения которого пока не существует. Фоторецепторы (палочки и колбочки) – специализированные нервные клетки, преобразующие свет в биологические электрические сигналы. При пигментном ретините происходит разрушение палочек и колбочек и замена их глиальной тканью.
Эксперименты показали, что как AAV2, так и AAV8 доставляют гены в сетчатку обезьян безопасно и эффективно, но для их доставки в фоторецепторные клетки AAV8 достаточно вводить в более низких дозах.
Ученые установили пороговые дозы для безопасного и эффективного таргетинга пигментных эпителиальных клеток и фоторецепторов. В то время как в пигментные клетки AAV2 и AAV8 эффективно доставляли ген GFP в дозе от средней до низкой, экспрессии этого гена в фоторецепторных клетках удалось достичь только при более высоких дозах. Значимая доставка гена GFP в палочки была достигнута при средних дозах AAV8, аналогичных тем, что в настоящее время используются в экспериментальных клинических протоколах.
(Laguna Design/Science Photo Library)
При введении в средних дозах вирусные векторы не вызывали у животных серьезных иммунных реакций и послеоперационных осложнений. Экспрессия доставленного в сетчатку гена отличалась очень высоким уровнем и оставалась стабильной на протяжении всего исследования – в течение четырех месяцев. Кроме того, ген GFP преимущественно трансдуцировался в один из типов ганглиозных клеток сетчатки, что удивило ученых. Ганглиозные клетки сетчатки передают зрительную информацию от сетчатки к нескольким областям мозга. Эти данные могут быть использованы для дальнейшего разграничения нейронных связей между сетчаткой и мозгом.
В более ранних исследованиях AAV8 уже доказал способность безопасно и эффективно доставлять гены в сетчатку мышей. Однако сетчатка мышей значительно отличается от сетчатки обезьян, в первую очередь, структурно, что оказывает влияние на хирургический подход к доставке корректирующих генов в различные части глаза. (Например, у мышей, в отличие от обезьян, нет макулы – структуры, используемой для зрительного различения). Исследование, проведенное на обезьянах, – следующий шаг на пути к успешному переносу вырабатываемых на животных терапевтических стратегий на организм человека.
«Результаты трех клинических испытаний I фазы на больных с врожденным амаврозом Лебера показали возможности генной терапии, основанной на аденоассоциированных вирусах, используемых в качестве средства доставки в сетчатку корректирующих генов», - отмечает соведущий автор статьи профессор кафедры офтальмологии Penn Джин Беннетт (Jean Bennett), MD, PhD. «Чтобы применять этот метод для лечения других наследственных глазных заболеваний, нам нужен более богатый векторный инструментарий, и то, что мы увидели при использовании AAV8, дает надежду на разработку методов лечения заболеваний, атакующих фоторецепторные клетки сетчатки. Эти исследования обеспечивают нас необходимыми данными для определения дозы и типа вектора для лечения слепоты, вызванной потерей фоторецепторов».
«Для лечения пациентов с другими заболеваниями сетчатки нам нужно оживление технологий – новые и более эффективные вирусные векторы для безопасной доставки корректирующих генов», - добавляет профессор Вилсон. «Моя лаборатория недавно выделила новые семейства обезьяньих адено- и аденоассоциированных вирусов. Рекомбинантные варианты этих вирусов, как оказалось, являются более совершенными средствами доставки генов к целому ряду мишеней».
По материалам
Next Generation Gene Therapy: Penn Study Demonstrates Potential of New Gene Vector to Broaden Treatment of Eye Diseases
Оригинальная статья:
L. H. Vandenberghe, P. Bell, A. M. Maguire, C. N. Cearley, R. Xiao, R. Calcedo, L. Wang, M. J. Castle, A. C. Maguire, R. Grant, J. H. Wolfe, J. M. Wilson, J. Bennett. Dosage Thresholds for AAV2 and AAV8 Photoreceptor Gene Therapy in Monkey
© «Ученые ищут, находят и изучают новые вирусные векторы для генной терапии». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Генная терапия. Письменное разрешение обязательно.
Related Articles: |













