|

Мертвое море. Вопреки распространенному мнению, оно совсем не мертво. Его заселяют микроорганизмы-галофилы, выработавшие в процессе эволюции уникальный метаболический путь, позволяющий им жить в экстремальных условиях чрезвычайно высокой солености.
(Фото с сайта fotki.yandex.ru)
При переработке органических веществ в качестве источника углерода для синтеза углеводов микроорганизмы Мертвого моря используют ранее неизвестный метаболический путь, дающий им возможность жить в условиях чрезвычайной солености. Открытие позволяет предположить существование и других неизвестных путей, необходимых для выживания в экстремальных условиях, а также подтверждает феномен горизонтального переноса генов.
Вопреки распространенному мнению, Мертвое море не мертво. Оно населено микроорганизмами, большинство из которых принадлежит к группе солеустойчивых (галофильных) архей. Археи (от греч. Archaĩos – древний) - одни из самых первых форм жизни на нашей планете. Им удалось выжить в особенно экстремальных условиях. Изучением характерных для этих микроорганизмов метаболических процессов, до сих пор ускользавших от внимания эволюционных биологов, занимается исследовательская группа из Института биологии II (Institute of Biology II) Университета Фрайбурга (University of Freiburg), Германия, во главе с доктором Иваном Бергом (Ivan Berg).
Для выработки энергии и основных клеточных строительных блоков все известные организмы усваивают соединения углерода. Человек и другие позвоночные делают это с помощью цикла Кребса, или цикла трикарбоновых кислот, в котором важную роль играет активная форма уксусной кислоты – ацетил-коэнзим А (ацетил-КоА).
Позвоночные неспособны превращать ацетил-КоА в малат, предшественник других молекул, таких как сахара, но многие растения и микроорганизмы, в том числе и галофильные археи, с успехом справляются с этой задачей с помощью либо глиоксилатного цикла, либо этилмалонил-КоА пути, который в 2007 году был открыт той же группой доктора Берга. Они же открыли и новый микроб (Haloarcula marismortui), одноклеточный микроорганизм домена археев, использующий третий, ранее неизвестный, метаболический путь.
Ученые поняли, что Haloarcula marismortui не может использовать глиоксилатный цикл, так как у него отсутствует важный фермент этого цикла – изоцитратлиаза. Не может он использовать и этилмалонил КоА путь, так как у него нет некоторых генов, необходимых для синтеза используемых в этом цикле ферментов.
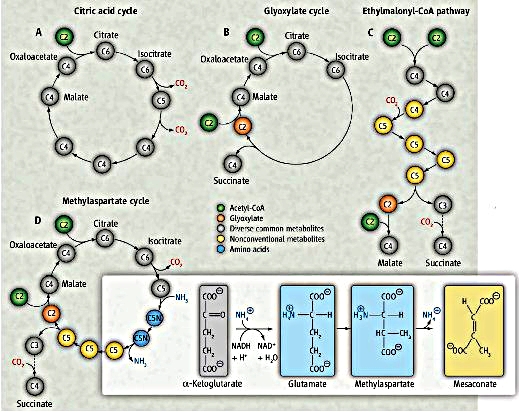
Пути ассимиляции ацетата. (Схема: sciencemag.org)
В течение двух лет исследователи анализировали ферменты H. marismortui, которые микроорганизм использовал при выращивании в среде, содержащей ацетат, и пришли к выводу о существовании еще неизвестного цикла, названного ими «метиласпартатным» (по названию одного из промежуточных продуктов цикла превращения ацетил-КоА в малат). В последнем номере журнала Science ученые описывают, как им удалось пролить свет на весь цикл реакций, включая все его промежуточные стадии, с помощью различных биохимических и микробиологических методов.
Метиласпартатный цикл длиннее и сложнее, чем два других пути, но он дает микробу, живущему при таком высоком уровне солености, ряд преимущества. Например, один из его интермедиатов ограничивает осмос, который в противном случае, пытаясь сбалансировать соленость, вывел бы из клетки воду.
Доктор Берг считает, что открытие третьего метаболического пути означает, что могут существовать и другие неизвестные циклы.
Открытия фрайбургской группы проливают некоторый свет и на эволюционные процессы, так как ферменты метиласпартатного цикла H. marismortui аналогичны обнаруженным у древних бактерий, но не присутствуют у других архей. Ученые задумались над тем, как возник этот метаболический путь в процессе эволюции, когда предки галофильных архей акклиматизировались к соленой среде обитания. К своему удивлению исследователи обнаружили, что гены метиласпартатного цикла предков солеустойчивых архей были «собраны вместе» из других микроорганизмов.
Феномен случайной передачи генов между организмами известен в биологии как «горизонтальный перенос генов». Однако ученые еще не наблюдали метаболический путь, целиком составленный из старых генов с различными функциями, представляющих совершенно различные метаболические пути, каким является метиласпартатный цикл. К новому метаболическому пути привела случайная (ре)комбинация всех этих старых генов у предка галофильных архей. Исследователи объясняют это тем, что в соответствии с принципом «эволюционного тинкеринга» (evolutionary tinkering) «изобрести» новые гены в результате длинной серии случайных мутаций гораздо сложнее, чем получить их, комбинируя уже существующие.
Суть концепции «эволюционного тинкеринга» сводится к тому, что эволюция – не искусный инженер, который все планирует и с самого начала точно знает, что он хочет создать. Биологи понимают эволюцию, скорее, как действия умельца, который находит импровизированные решения насущных проблем любым способом, каким только может. Умельцы необязательно используют новые части (или, говоря языком биологии, гены), а скорее берут все, что доступно и отвечает требованиям.
Принцип тинкеринга хорошо представлен французским генетиком лауреатом Нобелевской премии Франсуа Жакобом (François Jacob), который писал: «Естественный отбор... действует как "умелец", который не знает точно, что собирается соорудить, но использует все, что попадается под руку».
В экстремальных условиях этот принцип работает и при возникновении новых метаболических путей, что нашло свое подтверждение в исследованиях доктора Берга и его коллег.
По материалам
The Salt in the Soup of Evolution
Microbe processes carbon via new metabolic pathway
Аннотации к статьям
A Methylaspartate Cycle in Haloarchaea
Another Microbial Pathway for Acetate Assimilation

Related Articles: |













