|
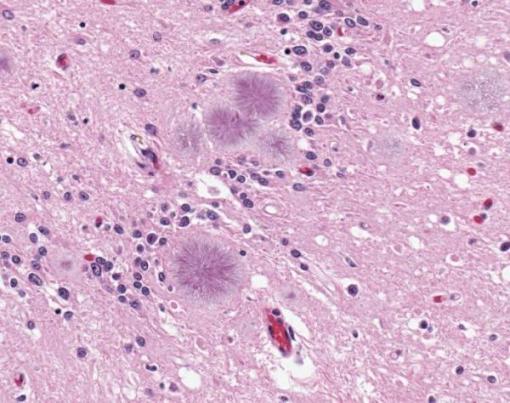
Микрофотография ткани мозга с типичными амилоидными бляшками при варианте болезни Кройтцфельдта-Якоба (vCJD). (Credit: Sherif Zaki; MD; PhD; Wun-Ju Shieh; MD; PhD; MPH)
Ученые Исследовательского института Скриппса (The Scripps Research Institute), Флорида, показали, что прионы, частицы инфекционных белков, способные вызывать фатальные нейродегенеративные заболевания, такие как коровья губчатая энцефалопатия, или «коровье бешенство», обладают способностью адаптироваться к новой среде клетки-хозяина.
В этом отношении, хотя у них и нет ДНК и РНК, они ведут себя так же, как вирусы, способные к различным самовоспроизводящимся структурным мутациям, обеспечивающим им очевидное эволюционное преимущество.
Исследование опубликовано в журнале Proceedings of the National Academy of Sciences.
«Мы обнаружили, что когда определенный штамм приона переносится из клеток мозга в другую клеточную линию, его свойства постепенно изменяются, приводя к формированию варианта штамма, более приспособленного к новой клеточной среде», - комментирует результаты работы руководитель отдела инфектологии доктор медицины и философии Чарльз Вайсманн (Charles Weissmann), возглавлявший исследование. «Если те же самые прионы впоследствии перенести в еще одну клеточную линию, они снова изменятся, адаптируясь к этим новым клеткам-хозяевам. Если прионы вернуть в клетки мозга, они постепенно восстанавливают свои первоначальные свойства. Мы нашли физическое подтверждения, по крайней мере, в одном случае, тому, что при изменении свойств приона изменяется и его сборка».
Эти новые данные появились примерно спустя год после того, как Вайсманн и его коллеги опубликовали исследование в журнале Science, в котором показали, что прионы способны эволюционировать в соответствии с теорией Дарвина.
Более раннее исследование уже показало, что прионы способны к частым мутациям и что эти мутации приводят к такой эволюционной адаптации, как резистентность к лекарственным препаратам – явление, ранее известное только у бактерий и вирусов. Последнее исследование также дает основания полагать, что нормальный прионный белок – встречающийся в клетках млекопитающих – может оказаться более эффективной терапевтической мишенью, чем его аномальный токсичный «родственник».
«Так как прионы могут адаптироваться к изменяющимся условиям внешней среды, сейчас становится ясно, что найти способные бороться с ними лекарственные препараты будет более сложной задачей, чем считалось ранее», - говорит Вайсманн. «Но если бы мы смогли разработать препарат, подавляющий образование нормальных прионных белков, мы, по существу, заставили бы инфекционные прионы голодать и не допустили бы их репродукции. Такой подход к лечению, хотя он и сложен технически, нельзя не иметь ввиду, так как, как мы показали ранее, потеря белка PrP не наносит вреда здоровью – по крайней мере, здоровью мышей».
Состоящие только из белков прионы классифицируется в различные штаммы, в зависимости от времени инкубации и вызываемых ими заболеваний. Кроме «коровьего бешенства» у крупного рогатого скота к болезням, вызываемым прионами, относят скрэпи у овец, хроническую кахексию у оленей и вариант болезни Кройтцфельдта-Якоба у людей. Прионы обладают способностью к воспроизводству, несмотря на то, что не имеют состоящего из нуклеиновых кислот генома.
Клетки млекопитающих обычно синтезируют клеточный прионный белок, или PrPC. При инфицировании аномальный, или неправильно собранный, белок - известный как PrPSc – превращает нормальный прионный белок клетки-хозяина в его токсическую форму, изменяя его конформацию. Терминальная стадия заболевания характеризуется образованием больших полимеров из таких аномально собранных белков, что приводит к массивному повреждению клеток и ткани.
«Инфекционный прионный белок может быть собран по-разному, и, в зависимости от его сборки, образуются разные штаммы», - объясняет Вайсманн. «Оставаясь в одном и том же хозяине, прионы сохраняют характерную для них сборку, так что штаммы воспроизводятся точно».
Однако при воспроизводстве сборка не всегда осуществляется правильно, поэтому популяция прионов состоит из многих вариантов белка, хотя их численность и находится на низком уровне.
Новое исследование показало, что если популяция прионов переносится в клетки другого хозяина, один из вариантов может реплицироваться более быстро – эволюционное преимущество – и стать доминирующим штаммом. Эта новая популяция также будет содержать в своем составе различные варианты, один из которых может быть отобран при передаче следующему хозяину.
«В результате, в том, что касается мутирования и эволюционного отбора, прионы, хотя и лишенные генетического материала, ведут себя аналогично вирусам и другим патогенам», - объясняет Вайсманн. «Они делают это, изменяя свою сборку, в то время как вирусы вносят изменения в последовательность своих нуклеиновых кислот».
Новое исследование позволяет предположить, что популяции прионов составляют «квази-виды», аналогичные по природе РНК-содержащим вирусам и ретровирусам, таким как вирусы гриппа и ВИЧ.
Идея квази-видов была первоначально предложена Манфредом Эйгеном (Manfred Eigen), немецким биофизиком, получившим в 1967 году Нобелевскую премию в области химии. По существу, квази-вид – это сложная самовоспроизводящаяся популяция различных и связанных между собой особей, функционирующая как единое целое. Однако именно Вайсманн в 1978 году нашел первое подтверждение теории, изучая один из бактериофагов – вирусов, инфицирующих бактерии – во время своей работы в качестве директора Института молекулярной биологии (Institut für Molekularbiologie) в Цюрихе, Швейцария.
«Но на этом сравнение заканчивается», - продолжает Вайсманн.
«Тот факт, что они ведут себя как вирусы, не означает, что они сами – что-то похожее на вирусы. Велосипед похож на автомобиль, если рассматривать его с той точки зрения, что он может доставить вас из одной точки в другую, но они не одно и то же. Тем не менее, конечный результат одинаков. Чтобы выжить, и прионы, и вирусы способны изменять свою структуру».
По материалам
Scripps Research Scientists Show Prions Mutate and Adapt to Host Environment
Аннотация к статье: Transfer of a prion strain to different hosts leads to emergence of strain variants
Еще о нейродегенеративных заболеваниях (Альцгеймера, Паркинсона, Гентингтона)
Источником бета-амилоидного белка при болезни Альцгеймера может быть печень, а не мозг
Синтезировано соединение, блокирующее разрушение клеток мозга при болезни Паркинсона
К созданию нанопор ученые подключили даже бабочек
Чистая популяция нервных стволовых клеток обещает значительный прогресс в лечении нервных заболеваний
Болезнь Хантингтона: неупорядоченные белки распространяются из клетки в клетку, приводя к прогрессированию заболевания
Причина болезни Хантингтона найдена в митохондриях
Подтверждена исключительная роль фермента AMPK в аутофагии и увеличении продолжительности жизни
Белки, связанные с нейродегенеративными заболеваниями, образуют бляшки в процессе нормального старения
Анализ крови для болезни Альцгеймера?
Сигнальный белок ревматоидного артрита излечивает болезнь Альцгеймера у мышей
Противодиабетический препарат метформин может оказаться эффективным средством лечения болезни Альцгеймера
Ученые установили одну из причин повреждения головного мозга при болезни Альцгеймера и нашли способ устранить ее
Белки сиртуины помогут улучшить память и способности к обучению
Ученые установили функции клеток головного мозга через 150 лет после их открытия
Простые низкомолекулярные соединения разрушают металло-амилоидные бляшки при болезни Альцгеймера
Определен ключевой белок регенерации нервных клеток
Физики изучают фермент, связанный с болезнью Альцгеймера и раком
Установлен белок, связывающий болезнь Паркинсона с некоторыми видами рака
Related Articles: |













