|
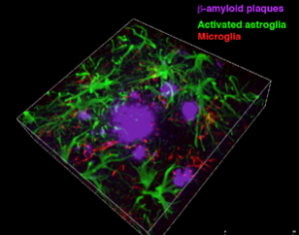
3D реконструкция амилоидных бляшек и астро/микроглиозиса. (Фото: Boston University School of Medicine)
Ответный удар по нейродегенерации
Клетки головного мозга, называемые микроглией, разрушают токсичные вещества и остатки мертвых клеток, подавляют воспаление и синтезируют вещества, необходимые нейронам. Новое исследование показывает, что, поддерживая их нормальную функцию, можно предотвратить нейродегенерацию.
Массовое отмирание нервных клеток в головном мозге людей, страдающих болезнью Альцгеймера, может в значительной степени быть связано с ослаблением функции совершенно другого класса клеток головного мозга, называемых микроглией, считают ученые Школы медицины Стэнфордского университета (Stanford University School of Medicine).
В экспериментах на мышах исследователи установили, что подавление активности одной из молекул на поверхности микроглиальных клеток восстанавливает их способность должным образом выполнять свою работу и обращает вспять потерю памяти и множество других характерных для болезни Альцгеймера когнитивных нарушений.
Исследование, опубликованное в журнале The Journal of Clinical Investigation, показывает важность микроглии и может привести к новым способам предотвращения болезни Альцгеймера, которой, по прогнозам, к середине века будут страдать 15 миллионов человек, если только не будет найден какой-либо метод ее лечения или профилактики. Кроме того, эта работа может помочь найти объяснение интригующей связи между аспирином и снижением скорости развития болезни Альцгеймера.
Клетки микроглии, составляющие около 10-15 процентов всех клеток головного мозга, фактически гораздо ближе к иммунным клеткам, чем к нейронам.
«Клетки микроглии – патрульные полицейские мозга», - говорит руководитель исследования Катрин Андреассон (Katrin Andreasson), MD, профессор кафедры неврологии и неврологических наук. «Наши эксперименты показывают, что не дать им свернуть с правильного пути значит оказать противодействие потере памяти и сохранить здоровую физиологию мозга».

Профессор Кэтрин Андреассон (Katrin Andreasson), MD. (Фото: Stanford University School of Medicine)
Микроглиальная клетка – часовой на передовой линии, отслеживающий подозрительную активность в зоне своей ответственности путем зондажа окружающей микросреды. Усмотрев нарушение, она высвобождает вещества, привлекающие другие микроглиальные клетки, поясняет профессор Андреассон. Эти клетки – жесткие полицейские, защищающие мозг от вторжения бактерий и вирусов. Кроме того, они эксперты по части «успокоения», подавляющие воспаление, если оно выходит из-под контроля. Помимо этого они работают «сборщиками мусора» – уничтожают мертвые клетки и разбросанные среди живых клеток молекулярные отходы, в том числе кластеры белка бета-амилоида, известного своей способностью образовывать липкие агрегаты. Такие агрегаты, называемые бета-амилоидными бляшками, являются характерной анатомической особенностью болезни Альцгеймера.
Бета-амилоид, синтезируемый по всему организму, настолько же естественен, насколько и вездесущ. Но когда он собирается в растворимые кластеры, состоящие из нескольких молекул, проявляется его чрезвычайно высокая нейрональная токсичность. Эти кластеры, как полагают, играют существенную роль в возникновении болезни Альцгеймера.
«Клетки микроглии должны, прежде всего, постоянно удалять бета-амилоид, а также держать в узде воспаление», - поясняет профессор Андреассон. «Если они теряют способность функционировать, ситуация выходит из-под контроля: бета-амилоид накапливается в головном мозге, вызывая токсическое воспаление».
Профессор Андреассон и ее коллеги получили убедительные доказательства того, что это нарушение функции микроглии вызывается, в значительной степени, повышенной сигнальной активностью одной из молекул на поверхности микроглиальных и нервных клеток. Предыдущая работа лаборатории Андреассон показала, что эта молекула, рецепторный белок EP2, обладает большим потенциалом вызывать воспаление при ее активации простагландином Е2, или PGE2.
То, что у биоинженерных мышей, клетки головного мозга которых лишены этого рецептора, активность воспалительного процесса в мозге значительно снижена, исследователи уже наблюдали. Но они не знали, какие клетки ответственны за эту воспалительную активность – нейроны или микроглия – и каковы ее конкретные последствия, и решили это выяснить.
Эксперименты начались в чашке Петри. Выделить из мозга жизнеспособные клетки микроглии достаточно сложно, в то время как собрать большое количество их близких родственников – иммунных клеток, называемых макрофагами, – значительно легче. Макрофаги циркулируют по всему организму, и их легко получить из образца крови. Не являясь копиями друг друга, клетки микроглии и макрофаги обладают многими общими генетическими, биохимическими и поведенческими характеристиками.
Помещенные в чашку Петри с растворимыми кластерами бета-амилоида макрофаги молодых мышей отвечали спокойно, синтезируя рекрутинговые химические вещества и не наращивая выработку воспалительных молекул. Следует отметить, что эти молодые клетки активно вырабатывали разрушающие бета-амилоид ферменты. Иная картина наблюдалась в экспериментах с макрофагами старых мышей: в этих клетках присутствие бета-амилоида провоцировало значительное усиление активности ЕР2, что, в конечном итоге, выражалось в усиленном синтезе воспалительных молекул и снижении выработки рекрутинговых химических веществ и разрушающих бета-амилоид ферментов.
Это первое указание на то, что возрастное изменение активности рецептора ЕР2 клеток микроглии может способствовать развитию некоторых из нейропатологических проявлений, имеющих непосредственное отношение к болезни Альцгеймера, нашло свое подтверждение в последующих экспериментах, в которых были использованы мыши, генетически предрасположенные к развитию аналога болезни Альцгеймера, а также нормальные мыши, в мозг которых ученые вводили либо бета-амилоид, либо контрольный раствор. Ожидаемое негативное воздействие на память и способность к обучению не проявлялось ни в одной из двух групп мышей, если, как результат генетических манипуляций, на клетках микроглии отсутствовал EP2. Подавление активности микроглиальных рецепторов ЕР2 значительно улучшало результаты, показываемые животными в двух видах стандартных тестов на память (в одном из тестов оценивалось, насколько быстро мыши забывает, что они уже сталкивались с каким-либо объектом раньше; в другом – способность запоминать местонахождение пищевой награды в лабиринте).
У мышей с избыточным количеством бета-амилоида, либо накапливающегося постепенно (мыши с «Альцгеймера»), либо появляющегося внезапно (мыши с инъекциями в мозг), и активированной бета-амилоидом микроглией нокаут функции EP2 очевидно улучшал память. Кроме того, при провокации мозга бета-амилоидом микроглия биоинженерных мышей, лишенная EP2, значительно превосходила неизмененную микроглию в выполнении таких важнейших задач, как секреция рекрутинговых химических веществ и факторов, полезных для нервных клеток, и синтез противодействующих, а не стимулирующих воспаление белков.
Эпидемиологические доклады свидетельствуют о том, что нестероидные противовоспалительные препараты, такие как аспирин, могут предотвратить развитие болезни Альцгеймера, хотя только в том случае, если их прием начинается задолго до проявления каких-либо признаков заболевания у пожилых людей, говорит Андреассон.
«Если у вас есть хотя бы малейший намек на потерю памяти, эти препараты не окажут никакого влияния», - подчеркивает ученый.
НПВП в основном работают за счет блокирования двух ферментов – COX-1 и COX-2. Эти ферменты создают молекулу, которая может быть преобразована в несколько различных веществ, в том числе PGE2 – гормоноподобное вещество, триггер активации ЕР2.
Хотя PGE2, как известно, регулирует воспалительные изменения в головном мозге, он выполняет различные функции во многих тканях организма – от влияния на кровяное давление до включения родовой деятельности. Еще более осложняет дело то, что PGE2 является лишь одним из пяти различных простагландинов, происходящих от молекулы-предшественника, производимой COX-1 и COX-2. Поэтому аспирин и другие СОХ-1- и СОХ-2-ингибирующие лекарственные средства могут иметь бесчисленные эффекты, не все из которых полезны. По мнению профессора Андреассон, может оказаться, что для защиты от болезни Альцгеймера без побочных эффектов лучше подойдет соединение, подавляющее активность ЕР2 только на клетках микроглии или таргетирующее какие-либо нижележащие последствия активности ЕР2. Ее группа уже занимается изучением биологических механизмов, посредством которых сигналинг PE2 сбивает с «пути истинного» клетки микроглии.
По материалам
Blocking receptor in brain’s immune cells counters Alzheimer’s in mice, study finds
Оригинальная статья
Jenny U. Johansson, Nathaniel S. Woodling, Qian Wang, Maharshi Panchal, Xibin Liang, Angel Trueba-Saiz, Holden D. Brown, Siddhita D. Mhatre, Taylor Loui, Katrin I. Andreasson. Prostaglandin signaling suppresses beneficial microglial function in Alzheimer’s disease models
Источник: NanoNewsNet
Related Articles: |













