Технологический прорыв, совершенный учеными Университета Райса (Rice University), США, может сделать обнаружение признаков болезни Альцгеймера таким же простым действием, как включение света.
Технология, о которой сообщается в журнале Journal of the American Chemical Society, должна помочь ученым в разработке более совершенных лекарственных препаратов для лечения этого разрушительного заболевания.
Лаборатория биоинженера из Университета Райса Анджела Марти (Angel Martí) занимается изучением молекул металлов, естественно взаимодействующих со скоплениями бета-амилоидных белков, образующих так называемые амилоидные волокна, из которых формируются бляшки в головном мозге пациентов с болезнью Альцгеймера. Когда такие молекулы, комплексы дипиридофеназина (dipyridophenazine) с рутением, связываются с амилоидными волокнами, их фотолюминесценция усиливается в 50 раз.
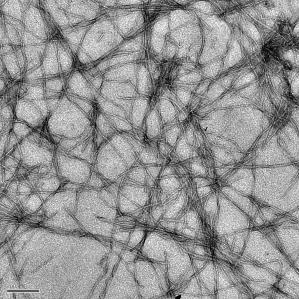
Амилоидные волокна (увеличенные на снимке в 12000 раз) считаются причиной образования бляшек в головном мозге пациентов с болезни Альцгеймера. Ученые Университета Райса создали молекулу на основе рутения с мощной фотолюминесценцией, проявляющейся при взаимодействии с амилоидными волокнами. (Фото: Nathan Cook/Rice University)
Благодаря значительному усилению фотолюминесценции такие комплексы могут стать альтернативой применяемым сегодня молекулам, используемым для изучения амилоидных волокон, которые, как считают ученые, образуются в результате скопления неправильно свернутых белков. Для описания перехода белка от неупорядоченных мономеров к агрегированным структурам ученые используют изменения во флуоресценции.
Натан Кук (Nathan Cook), бывший преподаватель Высшей школы Хьюстона (Houston high school), а ныне аспирант и ведущий автор новой статьи, начал заниматься бета-амилоидными белками, когда присоединился к лаборатории Марти, закончив курс по нанотехнологиям, преподаваемый профессором Университета Райса Джоном Хатчинсоном (John Hutchinson). Целью Кука было найти способ растворять амилоидные волокна в мозге пациентов с болезнью Альцгеймера.
Но когда он понял, что рутениевые комплексы, объект исследований группы Марти, имеют ярко выраженную способность люминесцировать при взаимодействии в растворе с амилоидными волокнами, он выбрал другое направление работы.
По словам Кука, амилоидные волокна несложно получить в лаборатории. Молекулы бета-амилоида естественно агрегируют в растворе так же, как и в мозге. Основанные на рутении молекулы, добавленные к мономерам бета-амилоида, не светятся. Но когда амилоиды начинают образовывать волокна, они напоминает «микроскопические спагетти» с естественно притягивающимися к ним гидрофобными частями металлокомплекса. «При изменении микросреды вокруг агрегированных пептидов изменяется и положение «переключателя», что позволяет рутениевым комплексам светиться при возбуждении спектроскопом», - объясняет Кук.
Красители на основе тиофлавина Т (ThT) - стандартные соединения для определения амилоидных волокон – работают аналогично. Но у тиофлавина Т есть недостаток: так как он возбуждается волной длиной 440 нанометров и излучает на волне 480 нанометров, разрыв составляет всего 40 нанометров.
Этот разрыв между длиной волны возбуждения и излучения известен как стоксов сдвиг. «В случае наших металлокомплексов стоксов сдвиг составляет 180 нанометров», – поясняет Марти, доцент кафедры химии и биоинженерии. «Мы возбуждаем комплекс волной длиной 440 нм, а излучает он почти в ближнем инфракрасном диапазоне – 620 нанометров. Когда нам нужно проводить скрининг препаратов, замедляющих рост амилоидных волокон, это становится преимуществом, так как некоторые из этих препаратов тоже флуоресцируют и могут скрывать флуоресценцию ThT, делая анализы ненадежными».
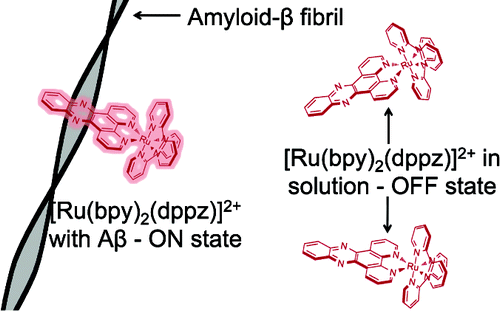
Агрегация бета-амилоидных пептидов связана с начальной стадией болезни Альцгеймера. Люминесцентный комплекс дипиридофеназина с рутением (II) может использоваться для мониторинга фибрилизации бета-амилоида. Этот комплекс не фотолюминесцирует ни в водном растворе, ни в присутствии мономеров бета-амилоида, но демонстрирует мощную фотолюминесценцию в присутствии скоплений бета-амилоидных волокон. Одно из его преимуществ состоит в большом стоксовом сдвиге (180 нм). Кроме того, продолжительное время фотолюминесценции позволяет использовать этот комплекс для определения фибриллярных белков в присутствии короткоживущих флуоресцентных фонов, используя технологию временного стробирования. (Рис. pubs.acs.org)
Долгоживущая фотолюминесценция рутениевого комплекса позволяет использовать «временное стробирования» спектроскопических анализов. «Мы специально взяли значения только от 300 до 700 наносекунд после возбуждения», - говорит Кук. «В этом диапазоне вся флуоресцентная среда в значительной степени исчезает, за исключением нашей. Замечательной частью этого эксперимента является то, что традиционные датчики оценивают флуоресценцию, главным образом, по двух параметрам – интенсивности и длине волны. Мы показали, что можно добавить третий параметр – время – и повысить разрешение флуоресцентного анализа».
По словам ученых, их комплексы могут особенно подойти для нового метода – так называемой флуоресцентной микроскопии в реальном времени (fluorescence lifetime imaging microscopy, FLIM), который различает микросреды скорее на основе продолжительности флуоресценции частицы, чем длины ее волны.
Цель Кука остается прежней – лечить болезнь Альцгеймера и, возможно, другие заболевания, например, болезнь Паркинсона – с помощью этого метода. Он видит возможность совместить свойство рутениевых комплексов специфически связываться с амилоидными волокнами с потенциалом других молекул растворять их.
«Это то, чего мы активно пытаемся достичь», - подтверждает Марти.
По материалам
Molecules 'light up' Alzheimer's roots
Аннотация к статье Sensing Amyloid-β Aggregation Using Luminescent Dipyridophenazine Ruthenium(II) Complexes













