|
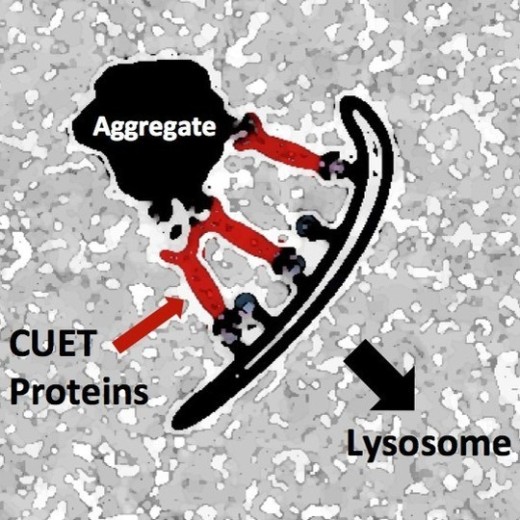
Вновь открытые белки, названные CUET-белками, (Cue5/Tollip адаптеры), показанные красным цветом, распознают патологические белковые агрегаты (клеточные отходы), в том числе, образующиеся при нейродегенеративных заболеваниях человека. CUET-белки также взаимодействуют со специфическими клеточными структурами, направляющими весь комплекс в лизосомы для утилизации и переработки. (Фото:Stefan Jentsch © MPI of Biochemistry)
Несколько нейродегенеративных заболеваний человека, в том числе болезнь Альцгеймера, болезнь Паркинсона и болезнь Хантингтона, а также и старение, связаны с накоплением в клетках аномальных и агрегированных белков. Клеточный «мусор» этого типа может быть удален из клеток их разрушением в лизосомах в процессе, известном как аутофагия. Ученые из Института биохимии Макса Планка (Max-Planck-Institut für Biochemie) в Мартинсриде, Германии, открыли новое семейство вспомогательных белков, распознающих помеченные для утилизации белковые отходы и эффективно направляющих их в лизосомы для разрушения и последующего рециклинга. Результаты этого исследования, опубликованные в журнале Cell, очень важны для понимания того, как клетки удаляют биохимические отходы, и открывают новые возможности в борьбе с нейродегенеративными заболеваниями.
Белки – составляющие нашего организма, выполняющие, контролирующие и организующие практически все функции клеток, – состоят из цепочек аминокислот, которые, как оригами, сложены в специфические сложные трехмерные структуры, соответствующие их функциям. Однако, поскольку фолдинг и сохранение таких структур очень чувствительны к внутри- и внеклеточным стрессам, свертывание белков может нарушаться и белки могут образовывать агрегаты. Такие нежелательные белковые отходы токсичны для клеток и могут вызвать их гибель. Так как, как известно, с накоплением аномальных белковых агрегатов связаны несколько нейродегенеративных заболеваний человека, результаты фундаментальных исследований, направленных на то, чтобы понять, как клетки удаляют биохимический мусор, имеют первостепенное значение для разработки стратегий профилактики и лечения таких заболеваний.
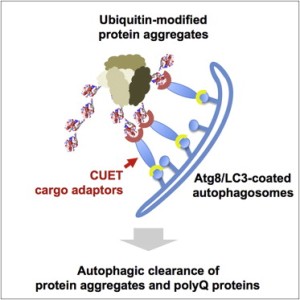
Селективная убиквитинзависимая аутофагия играет ключевую роль в элиминации белковых агрегатов, скоплений и органелл и противодействует цитотоксичности белков, связанных с нейродегенеративными заболеваниями. После субстратного убиквитилирования груз доставляется в аутофагосомы с участием таких адаптеров, как человеческий p62, которые связывают убиквитин и аутофагосомальный убиквитиноподобный белок Atg8/LC3. Однако существуют ли подобные пути у низших эукариот, оставалось неясным. Проведя скрининг дрожжевых клеток, ученые идентифицировали новый класс убиквитин-Atg8 адаптеров, названный CUET-белками, включающий в себя убиквитин-связывающий белок Cue5 с CUE-доменом у дрожжей и его человеческий гомолог Tollip. Cue5 взаимодействует с убиквитинлигазой Rsp5, и соответствующие дрожжевые мутанты накапливают имеющие тенденцию к агрегации белки и предрасположены к экспрессии белков PolyQ. Аналогично, снижение уровня Tollip повышает цитотоксичность, обусловленную PolyQ белками, в то время как гиперэкспрессия Tollip очищает человеческие клетки от связанных с болезнью Хантингтона белков PolyQ за счет аутофагии. Исследователи полагают, что CUET-белки играют важнейшую роль в устранении посредством аутофагии цитотоксичных белковых агрегатов и являются эволюционно древними. (Рис. Cell)
Для скрининга новых путей утилизации клеточных отходов ученые из лаборатории Штефана Йенча (Stefan Jentsch) использовали пекарские дрожжи. Кэфэн Лу (Kefeng Lu), постдокторант из Китая, открыл новый класс вспомогательных белков (названный CUET-белками), синтезируемых как в клетках дрожжей, так и человека, распознающих клеточный мусор, предназначенный для утилизации, по маркеру – белку убиквитину. Эти вновь идентифицированные хелперные белки транспортируют клеточный мусор по пути аутофагии к лизосоме – клеточному компартменту, предназначенному для разрушения и рециклинга. Кроме того, ученые показали, что вновь идентифицированным механизмом эффективно разрушается токсичный белок, связанный с аномальным образующим агрегаты белком болезни Хантингтона хантингтином. Существенно, что этот путь, по-видимому, специфичен для агрегированных белков подобных хантингтину и, очевидно, является более мощным, чем уже известные механизмы утилизации клеточного мусора.
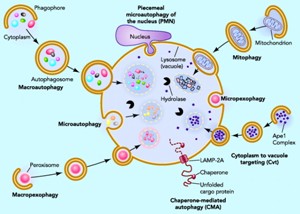
Три принципиально разных механизма аутофагии – макроаутофагия, микроаутофагия и микропексофагия. В зависимости от специфики груза аутофагия может быть селективным или неселективным процессом. При неселективной аутофагии часть цитоплазмы секвестрируется в двухмембранную аутофагосому, которая затем сливается с лизосомой/вакуолью. В противоположность этому селективное разрушение пероксисом при определенных условиях может быть достигнуто путем либо макро- , либо микроаутофагии, называемых макропексофагией или микропексофагией, соответственно. Поэтапная микроаутофагия ядра реализует деградацию части ядра. Кроме того, имеет место специфическая деградация митохондрий, называемая митофагией. Биосинтетический путь Cvt (cytoplasm to vacuole targeting) имеет аналогичные морфологические характеристики. Эти механизмы аутофагии характерны как для дрожжевых клеток, так и для клеток высших эукариот. Шаперон-опосредованная аутофагия (chaperone-mediated autophagy), по-видимому, имеет место только в клетках млекопитающих. (Рис. physiologyonline.physiology.org)
Поскольку вновь открытый механизм утилизации действует и у дрожжей, ученые могут в полной мере воспользоваться предоставляемыми этими клетками мощными экспериментальными возможностями для дальнейшего изучения нового пути. Детальный анализ этого механизма окажет значительное влияние на понимание того, как образующие агрегаты белки вызывают заболевания у человека, и будет способствовать разработке концепций их профилактики.
По материалам
Abfallentsorgung mit Relevanz für neurodegenerative Krankheiten
Оригинальная статья:
Kefeng Lu, Ivan Psakhye, Stefan Jentsch. Autophagic Clearance of PolyQ Proteins Mediated by Ubiquitin-Atg8 Adaptors of the Conserved CUET Protein Family
© «Открыт еще один механизм реализации макроаутофагии». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Нейродегенеративные заболевания. Письменное разрешение обязательно.
Related Articles: |













