|
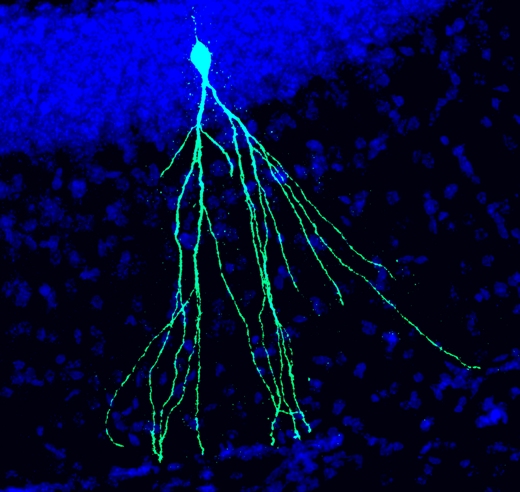
Недавно образовавшийся нейрон в мозге взрослой мыши. (Фото:© dkfz.de)
В Немецком центре исследований рака получили важную информацию о синдроме CHARGE
Синдром CHARGE* – тяжелое нарушение развития, поражающее многие органы. По данным мировой статистики, он встречается у одного из каждых 8500 новорожденных. Большинство из этих пациентов несут мутацию в гене CHD7. Как одна мутация вызывает такой широкий спектр характерных для CHARGE симптомов, до сих пор оставалось загадкой.
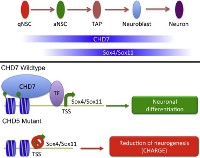
Ген CHD7 кодирует один из так называемых ремоделеров хроматина – важного класса эпигенетических регуляторов. Молекула ДНК наматывается на структуру, состоящую из гистоновых белков. Затем нить с похожими на бусины нуклеосомами скручивается в структуру, называемую хроматином. Чем больше нуклеосом занимает ген, тем он менее активен. Ремоделеры хроматина, такие как CHD7, играют важную роль в регуляции активности генов, так как создают в регуляторных последовательностях генов свободные от нуклеосом области. Таким образом, мутация в одном гене, кодирующем один из ремоделеров хроматина, может привести к неадекватной регуляции широкого спектра генов.
Лаборатория доктора Хайкунь Лю (Haikun Liu) в Немецком центре исследований рака (Deutsches Krebsforschungszentrum, DKFZ) занимается изучением регуляции взрослых нейральных стволовых клеток. Особое внимание ученые уделяют роли взрослых нейральных стволовых клеток в развитии заболеваний человека, в том числе умственной отсталости и опухолей головного мозга. Пациенты с синдромом CHARGE страдают умственной отсталостью и неспособны к обучению, что дает веские основания считать основой заболевания дефект центральной нервной системы.
Чтобы понять молекулярную роль мутации в гене CHD7 в фенотипе синдрома CHARGE, ученые использовали генетически модифицированных мышей. Вновь созданная модель дает возможность выключить ген CHD7 на определенных этапах развития только в нейральных стволовых клетках и проследить, как CHD7-дефицитные клетки пролиферируют, дифференцируются и созревают в течение всей жизни животного.
Эта работа дала удивительные результаты. При выключении CHD7, как в фетальных, так и во взрослых нейральных стволовых клетках, мутантные клетки вели себя одинаково: они теряли способность эффективно дифференцироваться в зрелые нейроны – основные функциональные единицы мозга человека и других животных. Зрелые нейроны в норме имеют очень сложную морфологию, что позволяет им создавать сети, имеющие важнейшее значение для обработки информации. Что касается мутантных нейронов с выключенным геном CHD7, то они, по-видимому, неспособны образовывать такие сети.
Но самым поразительным оказалось то, что физические упражнения полностью восстанавливают нормальный фенотип нейронов в гиппокампе – основной области мозга, ответственной за обучение и память. После тренировки на «беличьем» колесе – грызуны очень любят это занятие – CHD7-мутантные нейроны у CHD7-дефицитных животных полностью восстановились: они стали создавать функциональные сети.
Что бег вызывает резкое усиление нейрогенеза у взрослых, подтверждено как на животных, так и на человеке. «Мы очень рады, что последствия дефицита CHD7 в клетках можно обойти, задействуя неизвестный механизм, включаемый физическими упражнениями, в том числе, бегом. Теперь мы усердно работаем над поиском этого механизма», - комментирует результаты своего исследования доктор Лю.
Неврологи считает, что это открытие приведет к лучшему пониманию молекулярной основы синдрома CHARGE и, возможно, даже укажет способ реактивировать путь CHD7 и таким образом ослабить симптомы заболевания у человека.
Ген CHD7 связан и с развитием рака; мутации в этой молекуле присутствуют при многих различных типах раковых новообразований человека, включая рак легкого, толстой кишки и головного мозга. Вновь идентифицированный механизм дает этому четкое объяснение: мутация в CHD7 приводит к блокированию дифференциации стволовых клеток, что является основной причиной канцерогенеза.
Кроме того, ген CHD7 считается связанным с высоким риском развития аутизма, и у многих пациентов с синдромом CHARGE проявляются признаки этого заболевания. По-видимому, этот ген играет важную роль в регуляции и многих других физиологических процессов. По аналогии с исследованием на нейральных стволовых клетках, доктор Лю с коллегами планируют использовать свою прекрасную мышиную модель для изучения роли CHD7 в других типах клеток.
*Синдром CHARGE: колобома глаза (Coloboma of the eye), пороки сердца (Heart defects), атрезия хоан (Atresia of the choanae), выраженная задержка роста и развития (severe Retardation of growth and development), генитальные аномалии (Genital abnormalities), аномалии ушей (Ear abnormalities).
По материалам
Lauftraining lässt defekte Nerven-Stammzellen reifen
Оригинальная статья:
Weijun Feng, Muhammad Amir Khan, Pablo Bellvis, Zhe Zhu, Olga Bernhardt, Christel Herold-Mende, Hai-Kun Liu. The Chromatin Remodeler CHD7 Regulates Adult Neurogenesis via Activation of SoxC Transcription Factors
© «Физическая нагрузка восстанавливает нормальный фенотип нейронов гиппокампа». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Стволовые клетки.
Related Articles: |













