|
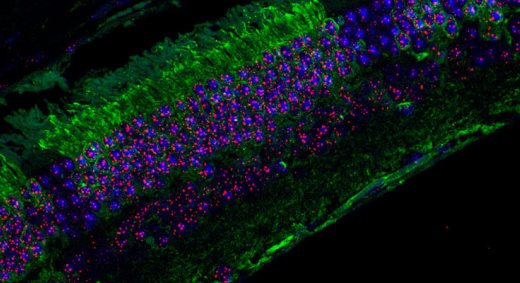
Глаз химерной мыши. В зеленых клетках – сверхдлинные теломеры (красные). (Фото: CNIO)
Добиться двукратного удлинения теломер можно без генных манипуляций
Группе ученых, занимающихся изучением теломер и теломеразы в испанском Национальном научно-исследовательском онкологическом центре (Centro Nacional de Investigaciones Oncologicas, CNIO), удалось создать мышей с сверхдлинными теломерами и замедленным молекулярным старением, не прибегаю к стандартному на сегодня методу – генетическому манипулированию. Новый метод, основанный на эпигенетических изменениях, описан на страницах журнала Nature Communications. Помимо замедления молекулярного старения это исследование предлагает новую стратегию получения эмбриональных стволовых клеток и индуцированных плюрипотентных стволовых клеток с длинными теломерами для использования в регенеративной медицине.
Теломеры (защитные структуры на концах хромосом) необходимы для стабильности генетического материала; они поддерживают наши клетки и весь организм в «молодом состоянии». Однако по мере старения теломеры становятся все короче и короче, и по достижении ими критической длины клетки входят в состояние сенесценции или умирают. Это одна из молекулярных причин клеточного старения и развития возрастных заболеваний.
Зато сверхдлинные теломеры – такие, как впервые полученные группой Марии А. Бласко (Maria A. Blasco), PhD, из CNIO путем усиления экспрессии гена теломеразы, – защищают от старения и связанных с ним заболеваний, значительно продлевая жизни мышей.
В 2009 году в журнале Cell Stem Cell появилась статья доктора Бласко и ее коллег о том, что in vitro культура iPS-клеток вызывает прогрессивное удлинение теломер (они были названы «сверхдлинными теломерами»). Немного позже, в 2011 году, Элиса Варэла (Elisa Varela), PhD, (также первый автор вышеупомянутой статьи) и ее коллеги из CNIO опубликовали статью в Proceedings of the National Academy of Sciences о том, что это спонтанного характера явление наблюдается и в культивируемых in vitro эмбриональных стволовых клетках. Это удлинение, которое происходит благодаря активным естественным механизмам без изменений в гене теломеразы.
Однако будут ли такие клетки способны развиться в мышь с более длинными, чем в норме, теломерами и с меньшей скоростью старения? В своей сегодняшней статье в Nature Communications доктор Варэла и ее коллеги утверждают, что это именно так.

Слева направо: Мигель A. Муньос-Лоренте (Miguel A. Muñoz-Lorente), Мария А. Бласко (Maria A. Blasco), Саграрио Ортега (Sagrario Ortega), Элиса Варэла (Elisa Varela), Агенда М. Техера (Agueda M. Tejera). (Фото: CNIO)
Судя по всему, клетки с сверхдлинными теломерами полностью функциональны. При анализе тканей в разные моменты жизни мышей (0, 1, 6 и 12 месяцев) в них сохранялась разница в длине теломер в сравнении с нормой (с течением времени теломеры укорачивались, но в обычной скоростью), накапливалось меньше повреждений ДНК и наблюдалась повышенная способность к устранению любого повреждения. Кроме того, у этих животных реже развивались опухоли.
Эти результаты позволяют предположить, что плюрипотентные стволовые клетки, несущие сверхдлинные теломеры, могут дать начало организмам, дольше остающимся молодыми на молекулярном уровне. По мнению исследователей, это «подтверждение концепции означает, что получать взрослые ткани с более длинными теломерами можно без генетических манипуляций».
«Кроме того, наша работа показывает возможность создавать iPS-клетки с более длинными теломерами, которые будут трансформироваться в дифференцированные клетки также с более длинными теломерами и которые поэтому будут лучше защищены» - добавляет доктор Бласко. «Это принесет пользу в регенеративной медицине».
Сейчас исследователи изучают, как использовать iPS-клетки для получения дифференцированных клеток для клеточной терапии, а следующим шагом будет «создание нового вида мышей, у которых теломеры во всех клетках будут вдвое длиннее, чем у нормальных», делятся планами Бласко и Варэла. Тогда они смогут заняться изучением некоторых важных вопросов, на которые пока нет ответа. Будут ли мыши – как биологический вид – с в два раза более длинными теломерами жить дольше? Является ли это тем механизмом, с помощью которого природа определяет разницу в продолжительности жизни генетически близких видов? Чаще или реже у мышей этого нового вида будет развиваться рак?
По материалам
Mice with hyper-long telomeres without altering the genes
Оригинальная статья:
Elisa Varela, Miguel A. Muñoz-Lorente, Agueda M. Tejera, Sagrario Ortega, Maria A. Blasco. Generation of mice with longer and better preserved telomeres in the absence of genetic manipulations
© «Добиться двукратного удлинения теломер можно без генных манипуляций». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Старение. Письменное разрешение обязательно.
Еще о работе Марии Бласко
Генная терапия: первый успех в увеличении продолжительности жизни
Ген Sox4 предотвращает развитие рака, но подавляет регенерацию тканей и ускоряет старение
Для регенерации кардиомиоцитов впервые применен фермент теломераза
и о старении
Низкомолекулярное соединение омолаживает стволовые клетки нескольких тканей
Старение и РНК-хеликазы
Форсированный апоптоз сенесцентных клеток увеличивает продолжительность жизни мышей
Роль митохондрий в старении клетки
Никотинамид рибозид останавливает процесс старения органов
Новое о гене Oct4. Может, он и есть тот самый ген «вечной молодости»?
Related Articles: |













