Устранить причину, а не симптомы: в шаге от победы над болезнью Хантингтона
(iStockphoto/Sebastian Kaulitzki)
Синтез мутантного хантингтина можно контролировать, не подавляя синтез нормального варианта белка
Болезнь Хантингтона, также известная как хорея Гентингтона, – наследственное нейродегенеративное заболевание головного мозга, вызывающее двигательные расстройства и деменцию. Обычно она проявляется в возрасте от 35 до 50 лет. На сегодняшний день заболевание неизлечимо и неизбежно ведет к смерти. Причиной болезни Хантингтона является специфический генетический дефект: в ДНК пациента – носителе генетической информации – присутствует чрезмерно большое количество определенного мотива.
«Подобные повторы присутствуют в ДНК и здоровых людей. Но в случае болезни Хантингтона эти последовательности длиннее, чем обычно», - объясняет руководитель исследования доктор Сибилл Краус (Sybille Krauß) из Немецкого центра нейродегенеративных заболеваний (Deutsches Zentrum für Neurodegenerative Erkrankungen, DZNE) в Бонне.
Чрезмерно длинные последовательности при болезни Хантингтона ведут к изменениям в определенном белке, известном как хантингтин.
«ДНК можно сравнить с архивом, в котором хранятся чертежи белков. Поэтому ошибки в ней приводят к синтезу дефектных белков. Хантингтин необходим организму. Это многофункциональный белок, играющий важную роль во многих процессах», - подчеркивает доктор Краус. «Если этот белок дефектен, клетки головного мозга могут умереть».
В своем исследовании доктор Краус и ее коллега – специалист в области генетики человека Сузанна Швайгер (Susann Schweiger) – сосредоточили свое внимание на одном из важнейших этапов синтеза белков – трансляции. На этом этапе информация с копии ДНК – матричной РНК – считывается в «фабриках по производству белка» – рибосомах. У пациентов с болезнью Хантингтона матричная РНК несет необычно большое количество последовательностей CAG (цитозин – аденин – гуанин) – код для синтеза аминокислоты глутамина. В результате хантингтин содержит так называемый амплифицированный полиглютаминовый тракт и, следовательно, дефектен.
Доктор Краус и ее коллеги идентифицировали комплекс из трех молекул, регулирующих синтез мутантного хантингтина. Снижение в клетке концентрации этого комплекса приводит к снижению синтеза мутантного белка.
Открытый немецкими учеными комплекс состоит из белка MID1, от которого он и получил свое название, и белков PP2A (protein phosphatase 2A) и S6K (40S ribosomal S6 kinase).
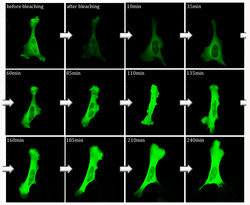
Молекулярные биологи изучили культуру клеток, синтезировавших мутантный белок хантингтин, связанный с болезнью Хантингтона. Эта серия изображений показывает такую клетку, исследованную с помощью метода FRAP (fluorescence recovery after photobleaching, восстановление флуоресценции после фотообесцвечивания). Как можно видеть, дефектный белок (помечен зеленым красителем) распространяется по всему телу клетки. После получения первого изображения связанный с уже присутствовавшими в клетке белками краситель был «выключен» («обесцвечен»), поэтому на короткое время интенсивность флуоресценции снизилась. Однако, когда в клетке были синтезированы новые белки, она опять усилилась. (Image by Nadine Griesche)
Для изучения влияния комплекса MID1 и взаимодействия его компонентов ученые провели серию сложных лабораторных экспериментов, занявшую несколько лет. Наряду с биохимическими методами исследователи использовали культуры клеток и анализировали белки мозга мышей. Генетический код мышей были изменен таким образом, что в нем появилось большое количество CAG-повторов, характерное для болезни Хантингтона.
Тенденция белка MID1 к связыванию с матричными РНК хорошо известна. Теперь же ученым удалось показать, что MID1 связывается и с РНК с чрезмерно длинными CAG-последовательностями. Кроме того, эксперименты показали, что в присутствии MID1 с РНК связываются и другие два компонента комплекса - PP2A и S6K – (в отсутствии MID1 этого связывания не происходит).
«Каждый из этих белков известен своей важной ролью в процессе трансляции. Мы установили, что при болезни Хантингтона они вместе связываются с последовательностью CAG. Раньше это не было известно. Кроме того, это связывание усиливается с увеличением длины повторов. При последовательностях нормальной длины связывание слабое или вообще отсутствует», - комментирует результаты работы доктор Краус. «Из этого можно сделать вывод, что эти три белка образуют взаимодействующий с РНК молекулярный комплекс, в котором MID1 является ключевым компонентом. Он, по-видимому, связывает весь комплекс воедино».
Более того, исследователям удалось доказать, что комплекс MID1 контролирует трансляцию РНК с чрезмерно длинными последовательностями CAG. Для этого они исследовали культуры клеток, синтезировавших либо нормальный хантингтин, либо его дефектный вариант. Концентрация MID1 в клетках была снижена с помощью генетической процедуры, известной как «нокдаун».
«Удаление этого белка, главной части комплекса MID1, имело прямое следствие: синтез дефектного хантингтина снижался. Однако это не оказывало влияния на выработку нормального хантингтина», - подчеркивает доктор Краус. «Это еще раз доказывает, что специфической мишенью комплекса MID1 является РНК с чрезмерно длинными CAG-последовательностями».
Доктор Краус видит в этом специфическом влиянии шанс на разработку метода лечения болезни Хантингтона: «Комплекс MID1 является перспективной мишенью для терапии. Он указывает на возможность подавления синтеза только дефектного хантингтина, без влияния на выработку нормального белка. Это следует подчеркнуть, потому что в организме пациента синтезируется и нормальный белок, очень важный для него. Если бы нам удалось найти способ воздействия на этот комплекс, например, с помощью фармацевтических препаратов, вполне возможно, мы смогли бы непосредственно влиять на синтез хантингтина. Такой метод лечения воздействовал бы не только на симптомы, но и на причину болезни Хантингтона».
Подходящее активное вещество пока не найдено. Однако в планах немецких ученых продолжение экспериментов: в ближайшее время они собираются проверить на такую активность ряд химических соединений.
По материалам
Forscher finden Steuerelement der Huntington-Krankheit
Оригинальная статья:
Sybille Krauß, Nadine Griesche, Ewa Jastrzebska, Changwei Chen, Désiree Rutschow, Clemens Achmüller, Stephanie Dorn, Sylvia M. Boesch, Maciej Lalowski, Erich Wanker, Rainer Schneider, Susann Schweiger. Translation of HTT mRNA with expanded CAG repeats is regulated by the MID1–PP2A protein complex
© «Устранить причину, а не симптомы: в шаге от победы над болезнью Хантингтона». Полная или частичная перепечатка материала разрешается при обязательной незакрытой от индексации, незапрещенной для следования робота активной гиперссылке на страницу Болезнь Хантингтона. Письменное разрешение обязательно.
Еще о болезни Хантингтона
Степень токсичности хантингтина может определяться белковым составом клетки
Два белка открывают новые перспективы в лечении болезни Хантингтона
На модели болезни Хантингтона временно восстановлена функция нейронов
Носители мутации болезни Хантингтона обладают лучшей способностью к обучению
Накопление хантингтина в клетках крови коррелирует со степенью атрофии мозга
Цинковые пальцы – новый инструмент в борьбе с болезнью Хантингтона
Синтетический митохондриальный антиоксидант подавляет симптомы болезни Хантингтона
Химические «выключатели» для нейродегенеративных заболеваний
Мутантный хантингтин изменяет паттерн химической модификации ДНК
Значительный прорыв в области лечения болезни Хантингтона
Related Articles: |













